基因剪刀手杨璐菡再创医学奇迹,猪器官也可移植到人体
 近日,Science在线刊登的一篇重量级文章《Inactivation of porcine endogenous retrovirus in pigs using CRISPR-Cas9》,一举攻克了将猪器官移植到人体内的关键问题,使得由猪拯救人类的日子变得更加近了。而该文章的通讯作者就是2017年全球青年领袖,80后科学家杨璐菡博士。
近日,Science在线刊登的一篇重量级文章《Inactivation of porcine endogenous retrovirus in pigs using CRISPR-Cas9》,一举攻克了将猪器官移植到人体内的关键问题,使得由猪拯救人类的日子变得更加近了。而该文章的通讯作者就是2017年全球青年领袖,80后科学家杨璐菡博士。 异种器官移植为何举步维艰?
异种器官移植为何举步维艰?
众所周知,人体作为一种复杂而精密的仪器,每一个零部件都发挥着不可替代的作用,而一旦其彻底坏掉了,器官移植就成为了救命稻草。显然,在如今科技飞速发展的今天,器官移植的成功率已经大大提高。
目前,器官移植所面临的最大困境就是器官移植供体的短缺。此问题在中国尤为严重,因为中国是全球器官捐献率最低的国家之一。据估计,2016年,每天都有22名患者在等待器官移植的过程中绝望的死去。
为了解决此难题,异种器官移植(xenotransplantation),即将动物器官移植到人体内,走进了人们的视野。经过无数次尝试及失败教训后,人们逐渐意识到,猪可能是人类理想的器官供体。
然而,猪器官移植的研究之路并不平坦。上个世纪90年代,猪器官移植一度在全球受到追捧,却又因猪的基因组里残留着PERVs(对猪没影响,却可能感染宿主)而受到重创,其临床试验被明令禁止,相关研究也停滞了近12年之久,成为了科学家搁置的领域。
魔剪CRISPR指出新方向!
随着魔剪CRISPR风靡全球,异种器官移植再次找到了新出路。杨璐菡所带领的研究团队就在含有DNA修复、促进细胞发育的“化学鸡尾酒”的基础上,以CRISPR技术对猪胚胎细胞内的PERVs的25个拷贝进行敲除,同时通过体细胞核移植技术成功获得了37只内源性逆转录病毒灭活的基因编辑猪。 世界上首批内源性逆转录病毒基因失活的幼猪
世界上首批内源性逆转录病毒基因失活的幼猪
毫无疑问,这项研究断绝了猪内源性逆转录病毒(PERVs)在器官移植接受者体内重新激活的可能性,加强了猪器官移植安全有效性,将异种器官移植技术向前推进了一大步,也为世上对匹配器官望眼欲穿的患者们带了极大的希望。
然而,杨璐菡表示,这还只是万里长征的第一步。很显然,PERV并不是猪器官异种移植的唯一挑战。未来,针对免疫系统相关基因进行修饰,以避免引发免疫系统排斥反应,则成为了杨璐菡研究团队的下一个需要攻克的难关。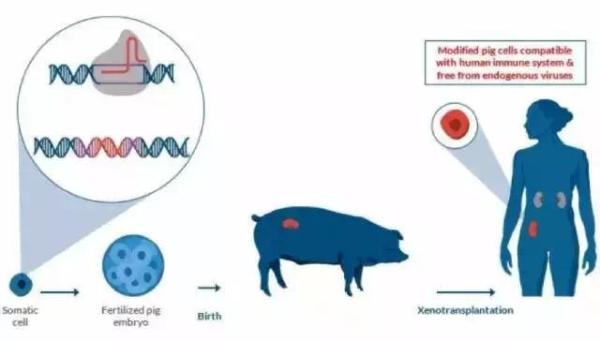
如何通过基因编辑技术实现安全的器官移植
科研界的女中豪杰:杨璐菡
其实,一直以来,对于猪器官移植这个问题,不管是过去还是现在都存在着令人生畏的障碍,然而,杨璐菡却无畏挑战,决心要为推动基因组技术的局限打开了一扇门,并要带领异种器官移植这个领域重新焕发蓬勃生机。
因而,她自哈佛大学获得博士学位后,师从有“合成生物之父”“基因编辑大牛”美誉的美国科学院与工程学院双料院士George Church教授,研究CRISPR-Cas9基因编辑系统,期望能通过该系统来改变异种器官移植的现状。
在攻读博士生期间,杨璐菡作为并列第一作者在Science杂志上发表了CRISPR-Cas9技术在细胞内修改基因组的工作,2011年至今,她已在《科学》、《NatureCommunications》、《NatureMedicine》等杂志上发表了数十篇论文,最高单篇引用数超过了3000。
2014年,杨璐菡和她的导师Church教授一起创立了一家名为eGenesis的生物技术公司,致力于推动异种器官移植临床应用。
2015年,他们通过CRISPR技术在细胞水平使猪基因组内62个PERV基因同时失活,证明了CRISPR技术有望解决猪器官异种移植所产生的挑战,同时也为此次针对猪胚胎细胞的基因编辑打下了基础。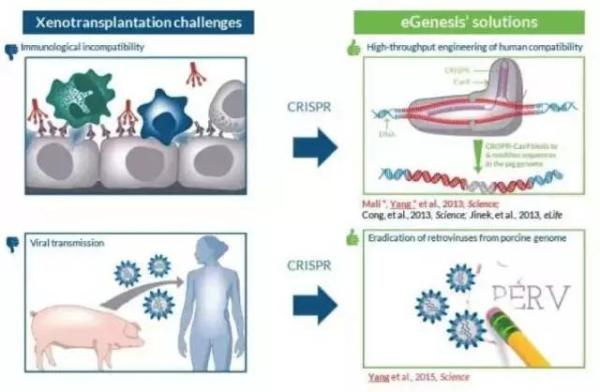
也正是因为这份出色的研究工作在以后会使世界上绝大多数人受益,出生于四川的杨璐菡于今年3月份被世界经济论坛评选为大中华地区的全球青年领袖之一,而且她是唯一一名来自生物技术与医学领域的被评选者。
与此同时,她和导师共同创立的生物技术公司eGenesis也获得3800万美元的融资,为后续利用CRISPR-Cas9基因编辑技术攻克人类器官移植的难题做了充分的准备。
杨璐菡表示,针对后续的免疫排斥问题,她的研究团队计划将CRISPR-Cas9技术与同源重组技术更好地结合起来,敲除不需要的基因,并引入新的基因,避免人体对这些器官产生排斥。
同时她也期望能利用这些资金打造一套能安全有效进行异种移植的方案,并在2018年至2019年期间真正进入临床,从而来造福有需要的患者。
也许,未来某天猪器官异种移植真的能改变全世界器官移植的面貌,就让我们拭目以待吧。

{replyUser1} 回复 {replyUser2}:{content}