深度解析:食药监总局不再保留,这意味着什么?
3月13日,一场重度雾霾,打破了人们对于全国两会气象保障工作的预期。
这一天,终于露出真容的《国务院机构改革方案》,在医疗领域的动作之大也打破了行业预期。
最高决策层以一种史无前例的方案,将国家药品监管部门置于新成立的国家市场监督管理部门之下。
忽如一夜春风来。柳暗花明又一村。健康点对药政、药审、立法、医改、行业协会等各方专家进行了多方访谈,以厘清此次改革的脉络逻辑。
“大市场”方案:力克跨部门推诿扯皮
不得不说,最新改革方案,让卫生系统的受访专家,有些猝不及防。
3月13日上午,受国务院委托,国务委员王勇就国务院机构改革方案向全国人民代表大会作说明。王勇透露,将国家食品药品监督管理总局(CFDA)等多部委的职责整合,组建国家市场监督管理总局,作为国务院直属机构。
在之前的坊间传闻中,分别存在两个主流方案:一个是“三局合一”的“大市场”方案,也就是国家工商总局、国家质监总局、国家食药监总局进行职能整合。另一个则是“大市场”和“大健康”方案,也就是国家食药监总局的药品、医疗器械监管职能划归国家卫生计生委管理,而食品监管划归新组建的国家市场监督管理总局管理。
方案揭晓后,国家食药监总局最终被确定并入新成立的国家市场监督管理总局,“大市场”方案成为现实。
这一改革方案其实已经有迹可循。在全国两会前夕,以中共中央名义印发的《关于深化党和国家机构改革的决定》,其中要求:“坚持一类事项原则上由一个部门统筹、一件事情原则上由一个部门负责,加强相关机构配合联动,避免政出多门、责任不明、推诿扯皮。”
2017年1月,国务院印发的《“十三五”市场监管规划》承认,市场秩序、市场环境还存在一些矛盾和问题,“假冒伪劣、虚假宣传、盗版侵权、价格违法行为和食品药品安全等问题多发”。
2017年2月,国家工商总局综合司司长袁喜禄透露,目前,全国有约1/3的副省级市、1/4的地级市、2/3的县实行了市场监管综合执法,采取工商、质监、食药监“三合一”的较为普遍,占一半以上,还有的是“四合一”、“五合一”的模式。通过机构整合、职能调整,综合执法改革取得积极成效:解决了部门间多头执法、权责不清等问题;优化了执法资源;提高了监管效能,减轻了企业负担;加强了基层机构和队伍建设。
但袁喜禄承认,工商、质监、食药监“三合一”还存在改革模式不统一;部门执法要求不一致;基层人员任务重、压力大;改革不配套不到位等问题。在各地试点层面上,省一级(不含直辖市)、国家一级当时尚未实现“三合一”。
从纵向看,过去40年间,国家药品监督管理局(SDA)、国家食品药品监督管理局(SFDA)的主管部委从原经贸委(现商务部)、原卫生部(现国家卫生计生委),直到2013年独立,成立正部级的国家食品药品监督管理总局(CFDA)。国家药监部门从未有与工商部门合并的先例。
从横向看,参与《药品管理法》立法咨询工作的中国药科大学研究生院常务副院长邵蓉教授坦陈,“至少在值得我们学习借鉴的国家,没有看到先例”。
健康点查阅17个国家的药品监管体制,它们或者作为内阁独立部门,或者隶属于国家卫生主管部门(作为独立国家局,或者附属司局),均未隶属于市场监管部门。
这些国家包括:美国、英国、日本、韩国、澳大利亚、加拿大、法国、德国、芬兰、荷兰、印度、马来西亚、新加坡、南非、瑞典、瑞士、爱尔兰。
这也正是医药、医疗领域受访专家的担忧所在:药品作为一种特殊商品,是否适合作为普通商品对其市场流通进行监管?
邵蓉在中南海举行的座谈会上,就直言“三合一”削弱了药品监管力量,淡化了药品监管事项。“因为药品有自己特殊的零售药店或医院渠道,药店也有自己的管理规则,医疗机构也有自己的监管部门。食品管理部门管的是生猪屠宰、小摊贩经营,两者完全不是一个层次。用药安全,人命关天。”
邵蓉进一步说,看待4年来的“三合一”改革,各地新成立的市场监管部门的负责人,通常是综合背景或者行政背景,对药品的安全性、风险管理的重要性并太不精通。而基层的药监执法队伍专业性,本身面临挑战。邵蓉说,各地药监局的一把手局长的药学专业背景的比例并不高,甚至一些地方药监局按政策接纳了转业军人作为执法人员,甚至担任局领导。
也许是注意到了业界担忧,最新改革方案明确:考虑到药品监管的特殊性,单独组建国家药品监督管理局,由国家市场监督管理总局管理。市场监管实行分级管理,药品监管机构只设到省一级,药品经营销售等行为的监管,由市县市场监管部门统一承担。
审评审批:成果还能固化吗?
作为一名“药学老人”,邵蓉见证了国家药监部门从原卫生部独立出来,首次作为国务院直属机构的一年。那一年,她36岁,是中国药科大学一位中青年教授。
在邵蓉看来,1998年机构改革的决策逻辑,更多着眼于科学执法、文明执法,改变民众对执法部门“白狼”“大黄狗”的不佳印象。至于制药产业界,当时对药监部门并没有特别大的期许。那一年,中国还是原料药、仿制药的天下,“创新度不高、转型要求不强烈,政策变化也没那么频繁,药企利润空间也比较大”。
然而,邵蓉认为,2013年以来,随着中国药品产业逐步与国际规则接轨,产业发展到一定阶段,也需要爆发点和转型期,要有很顺畅的审评审批通道,有协同的政策体系,产业界对药监部门的要求比20年前高多了。
工信部数据显示,2017年1-9月,医药工业规模以上企业实现主营业务收入22936.45亿元,同比增长11.70%。中国医药创新界讨论的不再是如何模仿一款国外畅销药,而是如何自主研发出一款创新药,至少也是通过跨国并购获得一款创新药的专利权。他们对时间的流逝日趋敏感,参与全球竞争的时间窗口,从若干年到一年,再到几个月,甚至是几十天。如果因为临床试验审批、医学伦理审查、人类遗传资源审批、新药上市许可审批,任何一个环节卡壳,就会让他们错过与全球同步研发、抢占上市先机的机会。
2015年,被中国医药产业界公认为是中国药品监管改革的新起点。这一年,国务院印发了《改革药品医疗器械审评审批制度的意见》。中国医药创新促进会执行会长宋瑞霖依然感受到中美医药创新的差距:中国改革开放快40年,我们的北斗卫星导航系统已经替代了美国的GPS,我们的高铁网络让美国相形见绌——谈到医药,我们真的不敢说什么。
这时,国家食药监总局迎来了一位新领导。曾任国家发改委副主任的毕井泉履新上任。一位熟悉毕井泉的医药界人士回忆道,当时,作为原国务院秘书长,毕井泉参与牵头了《“十二五”国家食品安全规划》和《“十二五”国家药品安全规划》的起草工作,还逼着国家食药监总局推进了仿制药一致性评价工作。国家食药监总局官员们,见到了一个强势的业务指导机构的领导,但很多人没想到,毕井泉会直接空降国家食药监总局,担任一把手。
在党中央、国务院领导下,国家食药监总局推动了一项被视为医药行业里程碑事件的大事——2017年10月,中共中央办公厅、国务院办公厅(简称两办)印发了《关于深化审评审批制度改革鼓励药品医疗器械创新的意见》(简称《创新意见》)。
2017年,在国家卫生计生委中国人口宣传教育中心指导下,健康点曾携手中国抗癌协会康复会共同发的一项研究显示,2017年8-9月,各有1/3被访者向课题组反映,难以了解最新的治疗方案(39%),国外创新药未在国内上市(36%),上市后部分创新药医院内配不到药(33%)是诊疗中的难点。创新药研究难、上市难、购买难,背后折射出临床研究、审评审批、临床应用的“三座大山”。
而《创新意见》正是剑指中国医药创新上、中、下游全链条。《创新意见》提出,明确了临床研究、临床试验、审评审批、集中采购、医保目录调整等一揽子的配套政策。甚至提出,对因临床试验和审评审批延误上市的时间,给予适当专利期限补偿……
随着作为改革纲领的《创新意见》颁布,从中央领导任务的有关主管部门,以两三天一份“红头文件”的速度,推进相关审评审批制度改革的落地。一位国家药品审评中心专家表示,牵头起草文件的国家药监总局(CFDA)及其国家药品审评中心(CDE),以及国家卫生计生委、国家人社部乃至中国人类遗传资源管理办公室,各方正在编制的实施细则、办法,多达数十份,“文件多到创新药企看不过来”。
正当食药监系统全周无休、熬夜加班做方案时,也许没有想到过,这个部门,即将被降格。
一位医改专家、一位药监立法专家和一位行业协会专家向健康点确认,按照3月13日的最新改革方案,作为新组建的国家市场监督管理总局代管的国家局,被摘掉“总”字的国家食品药品监督管理局(SFDA),将必须服从于国家市场监管部门党组的决定,并将丧失独立的部门规章立法权。
失去部门立法权意味着什么不言而喻。邵蓉指出,在2008~2013年之间,由于丧失了部门规章立法权,五年里,当时的国家食品药品监督管理局只修订了三个部门规章,并未出台任何重大药品监管新政。不过也有专家认为,2017年发布的《创新意见》,由中央深改小组亲自批准,代表党和国家的意志,原则方针不会随意出现反复。
一位不愿具名的药品审评专家说,政策稳定性,包括可预期性、透明性、连贯性,对药企是非常重要的影响因素。一款创新药报到国家药监部门进行审评审批,今年和明年的标准是否一致,这个主管和那个主管的标准是否一致,是全行业都关心的。
2018年3月,在“声音·责任”两会代表、委员座谈会上,医药界人士更多表达了对政策连贯性的渴望。全国人大代表、步长制药总裁赵超认为,政策的延续性尤为重要。创新药是高风险的产品,上级部门一旦确定了政策,不要出现一个领导一个部门一个想法,任何企业都没有能力去面对这样的政策。
新的“对手戏”:医疗与医保
尽管国家药监部门并未按照部分专家预期并入国家卫生计生委,但一款创新药要想进入国家基本药物目录,进入各省级集中招标采购平台,并最终进入各家医院临床医师的处方笺当中,就不可能不与卫生部门打交道。而这款创新药要想进入到国家基本医疗保险目录,又不可能不跟医保部门打交道。
就像“斗地主”的桌子还在,三个玩家全部换人。尽管改革方案仍然提出“三医联动”,但“三医”的主体——医疗、医药、医保,主管部门统统改变了。
在医疗方面,改革方案宣布成立国家卫生健康委员会,这是将国家卫生和计划生育委员会、国务院深化医药卫生体制改革领导小组办公室(国务院医改办)、全国老龄工作委员会办公室(全国老龄办)等职责进行整合。这被视为对2016年8月19日全国卫生与健康大会的中央精神的贯彻落实:推动实施健康中国战略,树立大卫生、大健康理念,把以治病为中心转变到以人民健康为中心。
患者安全,是医疗服务的底线。人类伦理,是医疗服务的高线。创新发展,是医疗服务的生命线。一位参与《健康中国2030规划纲要》研究制定的学者认为,国家卫生健康部门往往更关注医疗服务质量、患者安全、人类伦理,而医药创新界更关注科技创新和产业效益,改革后的国家药监部门如何与国家卫生健康部门协调,值得关注。
在医保方面,改革方案宣布成立国家医疗保障局,统筹推进医疗、医保、医药“三医联动”改革,成为兼具保险支付、药品定价的一个强势部门。新部门全面整合了城镇职工和城镇居民基本医疗保险、生育保险职责,新型农村合作医疗职责,药品和医疗服务价格管理职责,医疗救助职责整合。
无论是卫生部门还是药监部门,管的都是技术、安全,是准入的最低标准;真正影响医疗服务行为的,是医保补偿机制、价格机制、医院人事薪酬机制。多位受访的医药卫生界全国政协委员告诉健康点,如果这些机制没有理顺,光靠医保对医院“突击式控费”,2017年部分省份患者“看病被拒诊”“用药卡脖子”还会继续发生,而针对创新药的医保精细化管理,需要破题。
改革之路,仍然漫漫,司局级、处级机构职能整合的实施细则有待明确。上述专家表示,光靠体制内部的内生力量,是远远不足以推动改革的。
“一是市场的力量(群众的力量),二是中央的力量。这将是决定未来5年的根本力量。”这位专家最后说。
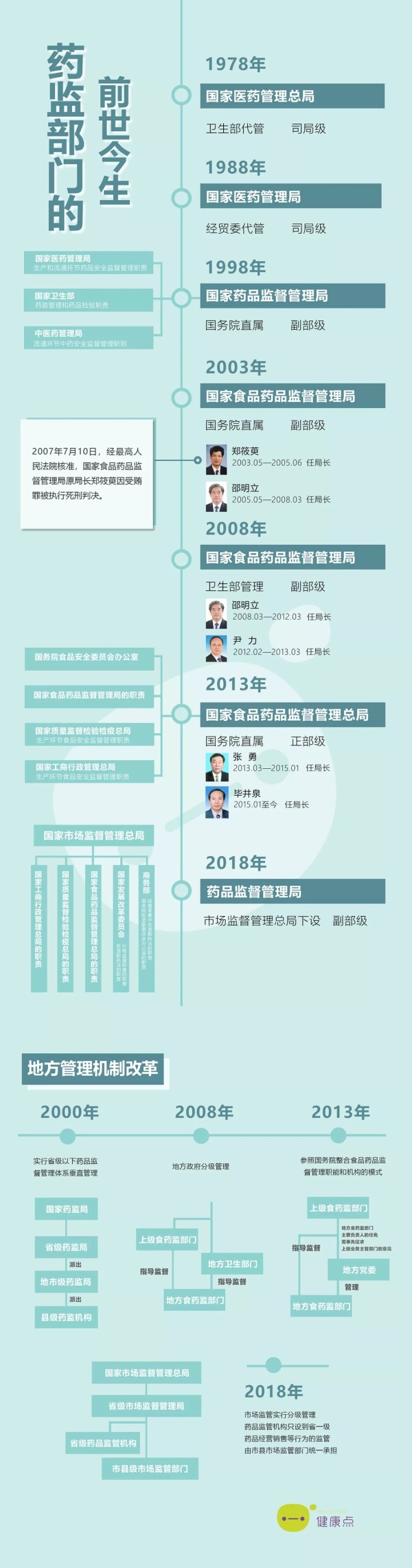
附:一图读懂“药监部门的前世今生”
文章来源:小桔灯网


{replyUser1} 回复 {replyUser2}:{content}