重磅级文章共同聚焦胰岛素最新研究成果 | 研究汇总
我们都知道,机体胰岛素能帮助调节血糖水平,而在糖尿病患者中这一功能或许被阻断了,近些年来科学家们将目光放到了胰岛素的研究上,本文中,小编就整理了近期与胰岛素相关的重要研究成果,分享给大家!
Neuronatin regulates pancreatic β cell insulin content and secretion
doi:10.1172/JCI120115
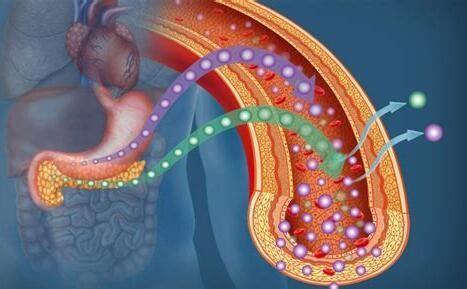
Neuronatin是一个印记基因可能参与人类肥胖,以激素和营养敏感性方式广泛表达在神经内分泌和代谢组织中。但是该基因的分子和细胞学功能以及在生理过程中的准确作用还没有得到完全揭示。最近来自英国的科学家们发现Neuronatin能够调节β细胞的胰岛素含量和分泌,并对其中的机制进行了深入研究,相关研究结果发表在国际学术期刊JCI上。
在这项研究中,研究人员发现在营养过剩的情况下,Nnat全身敲除小鼠和在β细胞中特异性敲除Nnat的小鼠都表现出葡萄糖刺激下胰岛素分泌的损伤,导致机体对葡萄糖的调节能力受损。相比之下,研究人员并没有发现Nnat全身敲除有任何进食和体重方面的改变。
【2】Hepatology:上海生科院发现治疗脂肪肝和胰岛素抵抗的潜在新分子
doi:10.1002/hep.29926
近日,来自上海生科院的李于研究员课题组在国际学术期刊Hepatology上发表了一项最新研究进展,他们发现肝脏CREBZF分子可能是治疗脂肪肝和胰岛素抵抗的潜在靶点分子。
胰岛素是负责脂肪酸从头合成的重要调控因子,在肝脏中促进葡萄糖转化成脂质。但是胰岛素信号如何转导进入细胞并调节脂质合成还没有得到完全揭示。
在这项研究中,研究人员发现ATF/CREB家族成员CREBZF通过胰岛素-Akt信号途径发挥作用,是调节脂质合成的关键因子。研究人员观察到,在再进食过程中,Insig-2a出现表达下调,导致SREBP1c发生进一步加工促进脂质合成,但是Insig-2a表达下调的机制还不明确。
新闻阅读:Alzheimer’s disease: why insulin is a new suspect
美国强生公司最近宣布,由于存在于一定的安全性问题,公司停止了一种新型阿尔兹海默病药物的临床试验,这是继多项大型临床试验宣布在治疗阿尔兹海默病上并没有效果的又一项失败的临床试验。越来越多的失败案例告诫我们似乎需要停下来思考一下我们是否找到了引发阿尔兹海默病的病因?
在对这种疾病第一次分析过程中,来自德国的医生Alois Alzheimer通过研究发现,死于这种疾病的患者大脑中会发生一些奇怪的变化,他并未在年轻人的大脑中发现两类蛋白质积累的状况,即存在于脑细胞之间的斑块(plaques)和脑细胞内部的缠结(tangles)。后期研究中,研究人员发现,由这种斑块组成的蛋白质是一种淀粉样蛋白(amyloid),而形成缠结的蛋白质则是tau蛋白,目前关于具体的结构研究人员仍然在争论之中。
【4】Diabetes:脂肪细胞和巨噬细胞对话介导胰岛素调控肥胖新机制
doi:10.2337/db17-1201
肥胖在全世界范围内的流行导致其逐渐成为一个公共健康问题,过多的能量摄入会转化成脂肪,特别是甘油三酯,储存在白色脂肪组织的脂肪细胞中。随着脂肪细胞中储存的脂肪越来越多,细胞体积越来越大,脂肪细胞会分泌促炎症脂肪细胞因子招募和极化巨噬细胞,引起慢性炎症导致肥胖相关紊乱。
之前在小鼠模型上进行的遗传学研究已经发现I型转化生长因子β受体(transforming growth factor-β receptor)——ALK7(activin receptor-like kinase 7)的功能丧失能够增加脂质分解抵抗脂肪细胞的脂肪累积。虽然研究已经证明在营养过剩的情况下GDF3(growth/differentiation factor 3)是ALK7的一个配体,但是GDF3的合成如何受到调控仍然不清楚。最近来自日本的科学家们发现胰岛素能够通过调节GDF3的表达影响脂肪细胞的脂肪分解过程和脂肪含量。相关研究结果发表在国际学术期刊Diabetes上。
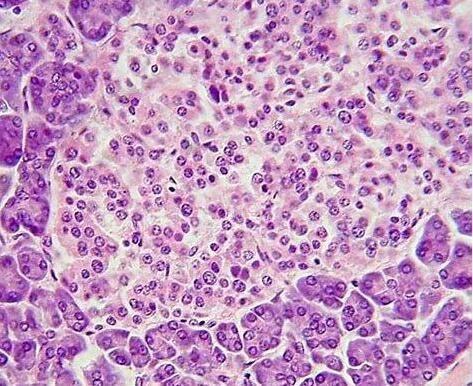
【5】Nat Commun:基因工程肾细胞在体内经咖啡因诱导后产生胰岛素
Caffeine-inducible gene switches controlling experimental diabetes
doi:10.1038/s41467-018-04744-1
在一项新的研究中,来自瑞士苏黎世联邦理工学院(ETH Zurich)、瑞士巴塞尔大学和法国普瓦捷-夏多落-尼奥尔工学院(IUT)的研究人员发现当接触咖啡因时,经过基因改造产生胰岛素的胚胎肾细胞能够降低糖尿病小鼠模型中的葡萄糖水平。相关研究结果于2018年6月19日在线发表Nature Communications期刊上,论文标题为“Caffeine-inducible gene switches controlling experimental diabetes”。
糖尿病患者血液中的葡萄糖含量高于正常水平,能够导致许多健康问题。目前的治疗方法包括让细胞对胰岛素更敏感的药物,或者注射胰岛素以便让需要它的细胞获得更多的胰岛素。在这项新的研究中,这些研究人员开发出一种新的方法来让身体在最需要胰岛素的时候获得更多的胰岛素。
【6】Diabetes:神经元调节胰岛素信号协调进食和葡萄糖平衡新机制
TCPTP Regulates Insulin Signalling in AgRP Neurons to Coordinate Glucose Metabolism with Feeding
doi:10.2337/db17-1485
胰岛素能够在外周组织以及脑部发挥作用调节葡萄糖代谢。胰岛素受体信号途径能够抑制位于下丘脑的AgRP神经元细胞促进胰岛素在外周对肝糖原合成的抑制,而AgRP神经元的激活会削弱棕色脂肪组织的葡萄糖摄取能力。之前的研究曾经发现酪氨酸磷酸酶TCPTP能够抑制AgRP神经元的胰岛素受体信号,饥饿的情况下下丘脑的TCPTP会被诱导表达,而进食后TCPTP则会被降解。
最近来自澳大利亚莫纳什大学的研究人员又评估了TCPTP在AgRP神经元中在控制葡萄糖代谢方面的作用。他们发现在AgRP神经元中特异性敲除TCPTP能够增强胰岛素敏感性,在高胰岛素-正葡萄糖钳夹过程中葡萄糖输注率增加,肝脏糖原合成减弱,同时伴随着棕色脂肪组织和棕色化白色脂肪组织葡萄糖摄取的增加。

【7】Diabetes:日本科学家发现调节胰岛素敏感性的新脂肪因子
SDF-1 is an Autocrine Insulin-Desensitizing Factor in Adipocytes
doi:10.2337/db17-0706
脂肪组织不仅是能量储存器官,也是重要的代谢调控器官,能够影响胰岛素敏感性和葡萄糖平衡。胰岛素抵抗不仅会发生在肥胖糖尿病状态下,在饥饿状态下也会出现,肥胖病人会出现胰岛素抵抗,是导致2型糖尿病发生的主要风险因素。对胰岛素敏感性的调节是生理代谢调节的重要方面,但是目前对调节上述两种胰岛素抵抗状况的分泌因子仍了解较少。最近来自日本的研究人员在脂肪细胞中发现了一个自分泌调节胰岛素敏感性的分泌因子,相关研究结果发表在国际学术期刊Diabetes上。
在这项研究中,研究人员利用数据库分析,体外和体内实验结合,发现SDF-1是脂肪细胞中参与胰岛素抵抗的一个因子,在饥饿状态和肥胖的脂肪组织中都会发生过表达。他们通过外源补充SDF-1发现SDF-1能够诱导ERK信号,导致脂肪细胞中的IRS-1发生磷酸化并降解,这会抑制胰岛素信号途径和葡萄糖摄取。
Insulin resistance causes inflammation in adipose tissue
doi:10.1172/JCI96139
肥胖诱导的胰岛素抵抗是2型糖尿病、高脂血症、心血管疾病和一些癌症类型发生的主要风险因素,肥胖引起胰岛素抵抗的机制到目前为止仍不明确。许多研究表明炎症与局部和系统性胰岛素抵抗的发生有关,特别是当炎症发生在白色脂肪组织当中,但是这些事件的因果关系还不清楚。在最近发表在国际学术期刊JCI上的一项研究中,来自瑞士的研究人员发现脂肪组织的胰岛素抵抗导致了局部炎症的发生,并非炎症导致了脂肪组织的胰岛素抵抗。
在这项研究中,研究人员利用Ap2-cre小鼠在脂肪组织中特异性敲除了mTORC2复合体的关键组成蛋白Rictor,阻断了脂肪组织中的胰岛素/mTORC2信号通路,在高脂饮食喂养下小鼠出现胰岛素抵抗,而蛋白质组学和GO分析结果表明,因mTORC2信号途径受阻断发生的胰岛素抵抗会引起促炎症巨噬细胞的局部聚集和炎症加剧。

【9】Cell Metab:脂肪细胞与免疫细胞对话共同影响胰岛素抵抗的形成
doi:10.1016/j.cmet.2018.02.007
内脏脂肪组织在调节全身能量平衡方面发挥多种作用,除此之外,最近一些研究表明内脏脂肪组织还为许多固有免疫细胞和适应性免疫细胞提供停留场所,直接参与免疫监视和宿主防御。
在最近发表在国际学术期刊Cell Metabolism上的一篇文章中,来自英国伦敦大学玛丽女王学院的研究人员报道称他们发现内脏脂肪组织中的传统树突状细胞(cDC)通过上调两条参与脂肪细胞分化的信号途径获得了一种耐受表型。
研究人员发现在cDC1这种树突状细胞亚群中Wnt/β-catenin信号途径的激活能够诱导合成IL-10,并上调cDC2亚群的PPARγ信号途径直接抑制它们的激活。这两条信号途径的联合作用会促进体内形成一种抗炎环境延缓肥胖诱导的慢性炎症和胰岛素抵抗的发生。而在长期营养过剩的情况下,脂肪细胞生物学的改变会影响β-catenin和PPARγ的激活,促进内脏脂肪炎症状态的形成。
【10】Endocrinology:德国科学家发现促进胰岛素分泌的新靶点
doi:10.1210/en.2018-00087
RabGTP酶激活蛋白TBC1D1已经被证明是骨骼肌葡萄糖和脂质代谢的关键调控因子,但是到目前为止该分子在胰岛中的作用还没有得到完全了解。最近来自德国的科学家们对该问题进行了研究,相关结果发表在国际学术期刊Endocrinology上。
研究人员表示他们想要在这项研究中揭示TBC1D1在胰岛细胞中对胰岛素分泌和底物利用的影响。他们首先从Tbc1d1缺失的小鼠体内分离出胰岛细胞并分析了葡萄糖刺激的胰岛素分泌和脂质代谢情况。从敲除小鼠体内分离得到的胰岛表现出GSIS的实质性增加,这归因于胰岛素分泌的第一和第二阶段的增强,并且胰岛素分泌的增强在葡萄糖的反复刺激下持续存在。


{replyUser1} 回复 {replyUser2}:{content}