全球首个大型动物研究证实:基因疗法有望根治肌萎缩
谁都希望自己的宝宝健健康康,但有些时候,偏偏会发生一些事与愿违的意外。遗传病就是这样的例子。看起来健康的夫妇二人,生下的宝宝却会出现奇怪的症状。直到做了基因检测才发现,宝宝是得了先天性遗传病。
在诸多遗传病里,杜氏肌营养不良大概是最为人所熟知的疾病之一。全世界范围内,大约有30万名儿童正饱受这种疾病的困扰,其中绝大多数是男孩。这是因为导致杜氏肌营养不良的基因dystrophin位于X染色体上,而男性基因组里又只有一条X染色体。因此一旦这个基因发生突变,就会导致疾病的产生。


▲本研究发表在了《科学》上,并得到了同期《科学》杂志的专题报道(图片来源:《科学》)
今天的顶尖学术期刊《科学》上,刊发了一项重量级的文章。来自德克萨斯大学西南医学中心的Eric Olson教授团队证实,利用CRISPR基因编辑技术,我们有望治疗,甚至是根治杜氏肌营养不良。这一设想已在大型动物中得到了验证。CRISPR技术的领军人物之一Jennifer Doudna教授在听到这则报道后表示“自己难以控制兴奋之情”。
那么,这项如此引人关注的突破,究竟是怎么完成的呢?这要从dystrophin基因的结构说起。在人体内,dystrophin是最大的基因之一,由79个独立的编码区域(外显子)组成。这就像是一幅巨大的拼图,每一块拼板都需要放对位置。一旦其中的某一块拼板出现突变,就可能会影响到整体的结构,最终影响基因功能。

▲这条基因的结构有点像拼图,需要每一块拼板的正确拼接(图片来源:Pixabay)
据统计,在杜氏肌营养不良患者里,第45号到第50号拼板间,很容易出现突变,这大概占了总体患者比例的13%。这些突变会让第51块拼板显得格格不入,怎么放都别扭。最后,细胞一怒之下,索性不去完成这幅拼图。这就导致了患者体内的关键蛋白缺失,引起症状。
了解了致病机理后,研究人员们开发出了一种新的方法。既然第51号拼板形状特殊,是个“刺头”,那我们直接跳过它,把52号拼板接上来,会发生怎样的结果呢?可喜的是,第52块拼板看上去是一个“百搭”,哪怕中间缺了几块,它也能和之前的拼板较好地融合。
▲美国FDA批准的Exondys 51,利用的就是“剔除刺头”的方法(图片来源:Sarepta Therapeutics)
那有人就问了,强行把52号拼板和其他拼板结合在一块儿,难道不会出事吗?许多研究表明这样的担心是多余的。的确,这样的做法会让dystrophin蛋白的成品里少掉几块拼板,但这总比没有强。而且,截短的蛋白,看起来功能也没有受到什么影响。基于这个原理,新药研发人员们已经开发出了一种叫做Exondys 51(eteplirsen)的疗法,并在2016年得到了美国FDA的加速批准,来到了患者身边。
说了这么多,故事看起来已经有了一个圆满的结尾,但我们还没有介绍这篇《科学》上的研究呢!回到eteplirsen这个疗法。尽管它能帮助患者重新产生dystrophin蛋白,但它的疗效究竟有多好,却一直是个讨论的热点。美国科学促进会(AAAS,也是《科学》杂志的主办者)在一篇报道中指出,在新型疗法的作用下,患者体内的dystrophin表达水平,大概只有正常水平的1%。它究竟能取得多好的疗效,也就因人而异了。
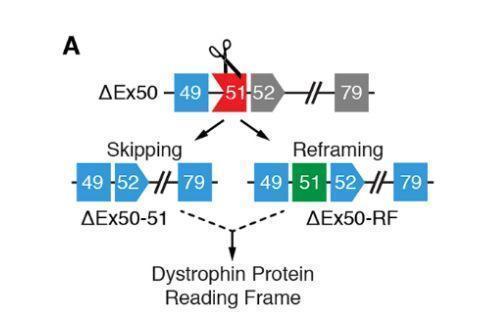
▲本研究的设计(图片来源:《科学》)
而这正是本篇《科学》论文的突破所在。首先,研究人员们选择了犬类模型,这些动物的dystrophin基因第50号拼板出现了突变。随后,研究人员们利用CRISPR基因编辑技术,在第51号拼板前切开了个小口子。而细胞为了修复这个小口子,会产生一系列潜在的效应。它有可能让第51号拼板的边缘变得顺滑,让它与第49号拼板顺利连接;也有可能让第51号拼板出现问题,使细胞在合成蛋白时也跳过它,而把49号拼板与52号拼板直接连在一起。
不管结局是哪一种,研究人员们都相信,这可以恢复dystrophin蛋白的生产。
而为了让身体里数十亿的肌肉细胞都能经过CRISPR的改造,研究人员们进一步使用了腺相关病毒(AAV)递送技术,把这套基因改造的系统送往全身各处。随后,他们使用免疫荧光技术,观察dystrophin蛋白的表达情况。荧光越强,就说明蛋白合成得越多。
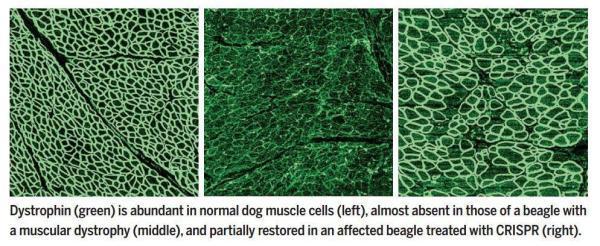
▲野生型(左)、突变型(中)、以及治疗组(右)的蛋白表达水平(图片来源:《科学》)
在所观察的两只实验组小狗中,研究人员们欣喜地发现,显微镜下,是一片绿色的荧光。初看之下,这与正常动物的表达水平极为接近。定量分析则发现,取决于肌肉细胞类型的不同,dystrophin的表达量范围是正常数值的3%-90%左右。而在心肌细胞内,高剂量的基因疗法,让dystrophin蛋白的表达量达到了正常值的92%!
为了获取实验数据,这些动物被实施了安乐死,因此我们无法得知它们是否能终身免于杜氏肌营养不良的症状,但Olson教授指出,这些“令人热泪盈眶”的发现开了一个好头。未来,他们也将扩大动物实验的规模,以求在人类试验前,获取足够多的安全信息。
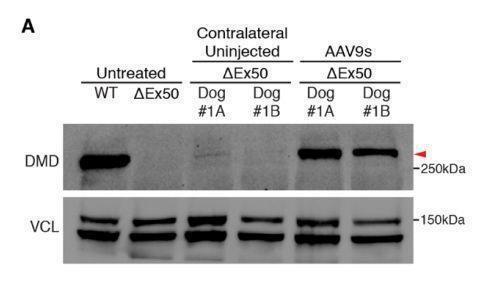
▲Western Blot也证实了动物体内产生了相应的正常蛋白(图片来源:《科学》)
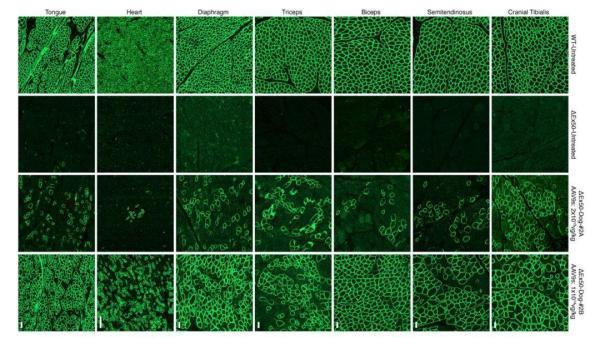
▲不同组织内的表达水平(图片来源:《科学》)
当然,即便这项研究能够转化为获批问世的疗法,它依旧有着一定的局限性。由于杜氏肌营养不良带来的症状是不可逆转的,患者需要在生命的早期接受治疗。此外,研究人员们也要通过长期研究确认,基于CRISPR的方法不会增加患者得癌症的风险。
但即便如此,这依然是诸多患者少有的治疗选择。在这个属于基因疗法的时代,CRISPR能带来多少惊喜?我们拭目以待!
点击“阅读原文”/“Read More”,即可访问原始论文页面。
本文题图来自《科学》。
参考资料:
[1] Gene editing restores dystrophin expression in a canine model of Duchenne muscular dystrophy
[2] In dogs, CRISPR fixes a muscular dystrophy
[3] Inch by inch, towards a treatment for Duchenne muscular dystrophy
来源:学术经纬
版权及免责声明:本网站所有文章除标明原创外,均来自网络。登载本文的目的为传播行业信息,内容仅供参考,如有侵权请联系答魔删除。文章版权归原作者及原出处所有。本网拥有对此声明的最终解释权。


{replyUser1} 回复 {replyUser2}:{content}