Nature子刊揭示CAR-T潜在风险,生产制造需谨慎
今日,发表于《自然》子刊《Nature Medicine》上的一项研究引起了业内的关注。来自宾夕法尼亚大学医学院的一支团队发现,充满颠覆性的CAR-T疗法,存在一个之前未经阐明的潜在风险。这也提醒我们在此类活细胞疗法的研发与生产中,需要慎之又慎。
CAR-T疗法是一类革命性的抗癌疗法。这种疗法的原理听起来很简单:医生们从罹患血液癌症(如白血病)的患者体内分离出免疫T细胞,对其进行基因改造,添加上针对癌细胞表面蛋白的CAR(嵌合抗原受体),使它们能攻击癌细胞。随后,这些细胞会被输注回患者体内,治疗癌症。
这一突破性的疗法在临床上取得了极好的效果。2017年,美国FDA批准了人类历史上的第一款CAR-T疗法。而最初在临床试验中接受CAR-T疗法的一名小女孩,至今已经6年多没有出现白血病的迹象,临床效果上等同于治愈。

接受CAR-T治疗后,小女孩Emily Whitehead已经多年无癌(图片来源:Emily Whitehead Foundation)
但我们也需要知道,这种基于活细胞的疗法非常复杂,而人类离理解其中的每一个细节,还有着一定距离。这也导致在实际治疗中,往往有一些出乎意料的情况发生。
今年5月,《自然》杂志上就刊登了这样一出“意外”。研究人员报道说,一名患者在接受CAR-T治疗的第50天,病情才出现起色。这对于要么快速起效,要么彻底无效的CAR-T疗法而言,显然是一个特例。这背后有着什么原因呢?
后续的研究发现,这名患者体内的CAR-T细胞,高达94%来自同一个祖先。回溯研究表明,在对T细胞进行基因编辑时,一条叫做TET2的基因被意外破坏,而它本身能抑制CAR-T细胞的增殖。换句话说,这个“美好的意外”让CAR-T细胞快速增殖,消灭癌症。如今,这名患者已经5年无癌。
但今日发表于《Nature Medicine》上的这个发现,则从反面揭示了CAR-T疗法的一个潜在风险。在这项研究中,一名B细胞急性淋巴性白血病(ALL)患者接受了一款成熟的CAR-T疗法,病情很快得到了控制。后续的研究也表明,他体内的CAR特异序列有保持高位。在一般情况下,这意味着CAR-T细胞的数量也处于高位,但奇怪的是,对细胞数目的统计却显示出了截然不同的结果——这些CAR特异序列的增加,和CAR-T细胞的数量看似无关。
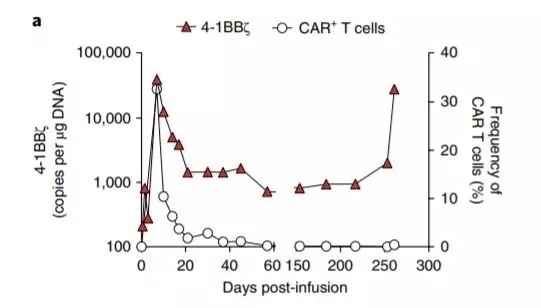
CAR特异序列的数量,与CAR-T细胞的数量没有相关性
在治疗短短9个月后,这名患者的白血病突然复发。而对这名患者血液样本的进一步分析,却揭示了一个令人不安的结果。这些CAR的特异序列,竟然来自癌细胞!而由于病情过重,这名患者最终也离开了人世。
这些CAR序列是怎么进入癌细胞的呢?研究人员们做出了两个假设。其一是依旧带有复制活性的慢病毒在体内侵入了癌细胞,另一种是在CAR-T疗法制备过程中的潜在污染。在治疗过程中,研究人员会对患者的血液样本进行定期检查。而对于这些样本的复查表明,后者更有可能是问题的根源。
那么这些在癌细胞表面表达的CAR,是不是复发的原因呢?很有可能。按照设计,这款CAR-T疗法针对的是癌细胞表面的的CD19蛋白。一旦癌细胞自己获得了CAR序列,就可以让自己的CAR与CD19蛋白互相结合,却不引发免疫反应。这等同于把自己的CD19隐藏了起来,让原本有效的CAR-T疗法,失去了自己的追踪目标。
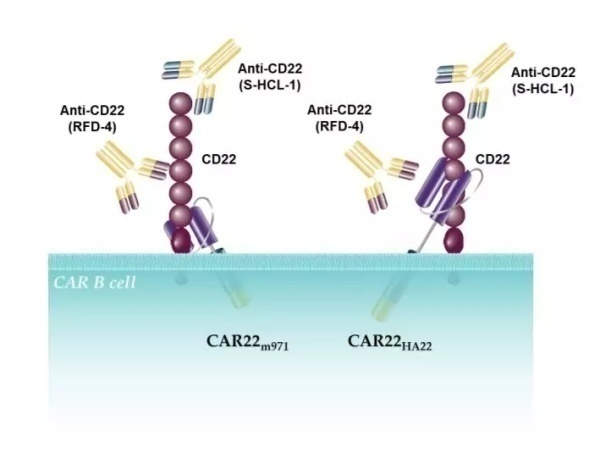
这种隐藏效果对其他CAR-T疗法也同样可能生效
“在这个案例中,我们发现100%的复发白血病细胞里,都带有我们用来修饰T细胞的CAR,”本研究的第一作者Marco Ruella教授说道:“这是在宾夕法尼亚大学接受治疗的数百名患者中,出现的首个案例。这也表明复杂的生产过程中,任何轻微的变动,都会对患者预后造成影响。”
“无论是成功还是失败,我们从每一名患者身上都学到了很多,” 本研究的通讯作者之一J. Joseph Melenhorst教授说道:“这是一个个例,但却非常重要。它能让我们重新思考制造CAR-T疗法的复杂流程,确保能带来长期的缓解。”
需要说明的是,CAR-T疗法依旧是一种极具突破性的抗癌疗法。本项研究的结果,并不能将其取得的成绩一笔勾销。相反,我们期待科学家们能从这个失败案例中学习到新的洞见,让未来的CAR-T疗法变得更安全,让更多患者从中受益!
来源:学术经纬
版权及免责声明:本网站所有文章除标明原创外,均来自网络。登载本文的目的为传播行业信息,内容仅供参考,如有侵权请联系答魔删除。文章版权归原作者及原出处所有。本网拥有对此声明的最终解释权。


{replyUser1} 回复 {replyUser2}:{content}