新进展!Nature:“先激活后绝杀”对抗艾滋 动物试验初见成效
9月底,《Nature》期刊发文揭示,联合两种广泛性中和抗体对抗艾滋病,能够一次性抑制艾滋病病毒数月之久。10月3日,这一顶尖期刊再次发表了艾滋病领域的又一进展:科学家们研发出新的组合策略,能够“先激活后绝杀”(Shock and kill)休眠的HIV。
抗逆转录病毒疗法(ART)的出现让艾滋病逐渐朝着慢性病的方向发展。但是,现有药物依然无法完全清除潜伏的HIV——它们会以不复制、休眠的状态寄生于CD4+T细胞中。一旦患者停止用药,这些潜伏病毒则有重新复制、入侵的风险。这意味着,要想真正治愈艾滋病必须跨过“潜伏病毒”这一难关。
为此,来自哈佛医学院的Dan H. Barouch教授带领团队给出一种新的尝试:他们研发出一种双管齐下的方法,已经在患有艾滋病的猴子身上得到证实。

https://doi.org/10.1038/s41586-018-0600-6
“先激活后绝杀”
“先激活后绝杀”(shock and kill)是针对潜伏病毒的主流策略,主要思路是:首先,利用药物激活潜伏在T细胞内的病毒使其暴露,随后通过增强免疫系统或者抗病毒 药物消灭携带病毒的宿主细胞。
在最新研究中,Dan H. Barouch团队选用了两种药物:
1)GS-9620(vesatolimod),一种口服药物,能够激活TLR7蛋白(Toll-like receptor 7),TLR7反过来会激活免疫系统,包括CD4+ T细胞、CD8+ T细胞以及NK细胞,后两种负责猎杀并摧毁受病毒感染的细胞。
2)PGT121抗体,该抗体的一端区域负责识别并结合受感染细胞表面的关键HIV蛋白,另一端区域负责激活免疫细胞,以摧毁受感染细胞。
动物试验:结果积极
Borducchi团队用HIV和猿类免疫缺陷病毒的混合型病毒感染了44只猴子。7天后,他们开始使用类似于人类的抗逆转录病毒 药物的有效组合来治疗这些感染动物。正如预期,艾滋病病毒迅速从所有猴子的血液中消失。
96周后,研究人员将猴子随机分成4组(每组11只)——其中,第一组不接受干预,第二组注射GS-9620,第三组注射PGT121,第四组同时注射GS-9620和PGT121。
猴子们接受这些治疗直到第114周,随后继续接受抗逆转录病毒治疗直到第130周,最后停止用药,等待病毒是否反弹。
结果显示,在停止抗逆转录病毒治疗后的21天内,研究人员在第一组猴子(没有接受药物/抗体干预)血液中均检测到了HIV。第二组(只接受GS-9620)中有10只猴子以及第三组中(只接受PGT121)有9只猴子同样检测到病毒。惊喜的是,第四组猴子,即同时接受GS-9620和PGT121的动物们,只有6只在ART停用后的第28周出现了病毒反弹的迹象。其他5只即便使用敏感的化验方法仍然没有检测到HIV。
为什么这种方法如此有效?研究团队发现,接受GS-9620的猴子体内的CD4+ T细胞和NK细胞都被激活了。但是仅仅激活这些细胞显然并不能够摧毁受感染的细胞,因为仅使用GS-9620治疗并不能阻止病毒反弹。更重要的是,GS-9620还能激活潜伏的病毒,使其从藏身之处“显露”出来,以便免疫系统能够锁定目标。而PGT121抗体则负责与激活的感染CD4+ T细胞上的病毒蛋白结合,以便激活的NK细胞能够攻击被感染的T细胞。
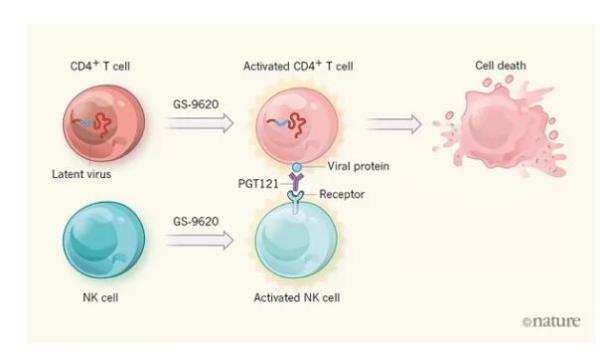 联合使用GS-9620药物和PGT121抗体“先激活后绝杀”(Shock and kill)病毒库的策略图
联合使用GS-9620药物和PGT121抗体“先激活后绝杀”(Shock and kill)病毒库的策略图
研究人员强调,动物试验有很理想的部分,例如在感染后几天内就开始抗病毒治疗(这对于艾滋病患者而言很难实现),在停止抗逆转录病毒治疗后这些猴子只被跟踪了大约6个月(艾滋病患者病毒反弹的时间可能会延迟2年)。
研究团队期待,GS-9620和PGT121(或者其他相关抗体)是否能够在患者身上也产生类似的结果。他们正在计划相关临床试验。同时,目前抗逆转录病毒 药物仍然是长期治疗艾滋病的最佳和唯一选择。
来源:CPHI制药在线
版权及免责声明:本网站所有文章除标明原创外,均来自网络。登载本文的目的为传播行业信息,内容仅供参考,如有侵权请联系答魔删除。文章版权归原作者及原出处所有。本网拥有对此声明的最终解释权。


{replyUser1} 回复 {replyUser2}:{content}