全球首款siRNA药物上市 后来者还有谁?
2018年8月, 全球首款 siRNA药物即Alnylam公司的Onpattro (Patisiran)由FDA批准上市,用于由 hATTR 引起的多发性神经病患者的治疗。
Onpattro是全球第一例依据诺贝尔奖成果 RNA 干扰技术开发的药物,1998 年,Andrew Fire和Craig Mello在线虫中首次揭示了RNAi现象,并凭借这一发现于2006年获得了诺贝尔生理学奖,到 2018 年首个 siRNA 药物的获批,历时20年的时间。Onpattro 的获批,标志着RNAi药物领域的重大突破,小核酸药物终见曙光。
技术突破成就的全球首款siRNA药物
据统计,在人体内的疾病相关蛋白中,大约超过80%的蛋白质不能被目前常规的小分子药物以及生物大分子制剂所靶向,属于不可成药蛋白。旨在通过基因的表达、沉默等功能治疗疾病的基因治疗被业界认为是继化学小分子药物、生物大分子药物之后的第三代治疗药物,这种疗法在基因水平上实现对疾病的治疗,不受不可成药蛋白的制约。作为基因治疗中RNA药物最主流的类型,siRNA 药物是从 mRNA 的水平对疾病进行治疗,相比化学小分子药物及生物大分子药物在蛋白质水平的治疗具有更高的效率。
2004年,美国Opko 公司开发的siRNA 药物Bevasiranib开展了用于湿性老年黄斑变性治疗的临床试验,这是全球首次与siRNA 相关的临床实验。随后,包括辉瑞、赛诺菲、罗氏及默沙东等在内的众多全球制药巨头纷纷加入到了siRNA 药物的开发队列中。
不幸的是,Bevasiranib项目的开发因临床效果欠佳而折戟于III 期临床中,其他后来者也未能幸免。究其原因,RNAi药物内在的靶向性差、脱靶效应及稳定性问题是影响其疗效的最主要制约因素,诸多因素导致这类药物治疗的效果远不及预期,同时还伴随着严重的无法克服的药物不良反应。
从技术需求的角度而言,静注后的siRNA易被核酸酶降解、肾清除率高、细胞摄取效率差,临床应用受到限制, siRNA 药物的成功有赖于药物递送系统技术的发展,尤其是能够将RNAi 安全、高效地转运至机体特定治疗靶位的递送载体技术。
作为全球首个获批上市的 siRNA药物, Patisiran 采用的LNP 给药系统将 RNAi 药物闭合包裹于脂质体内,可通过静脉注射的方式给药,脂质体的包裹大大提高了药物的稳定性以及对肝脏组织的靶向性,可以保证 siRNA 不被肾脏过滤清除,在血液循环的过程中逐渐被肝脏组织靶细胞所摄取,这是 Patisiran 克服上述主要制约因素进而获批上市的关键所在。
全球在研siRNA 药物进度概览
2013 年初,罗氏和Isis 达成一项3.92 亿美元的RNAi 药物交易,2014 年初又支付4.5 亿美元收购RNAi 专业研究公司Santaris;2014 年,赛诺菲以7 亿美元收购了小核酸药企Alnylam 12%股份。
种种迹象显示,技术发展带来的变革逐渐使得RNAi 药物的开发走出了发展初期的寒冬,相关药物的开发又逐步成为资本热捧的领域。截至目前,全球已经有多款 siRNA 药物处于临床阶段,在Onpattro之后,Alnylam公司用于急性肝卟啉症治疗的Givosiran 、Quark/苏州瑞博生物合作开发的视神经病变治疗药物QPI-1007及Quark在研药物QPI-1002用于急性肾损伤适应症都具备成为后续获批上市品种的潜力。
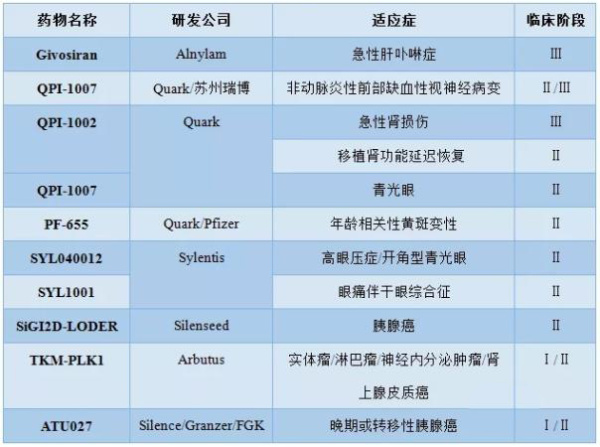
国内进展最快的siRNA 在研药物
在国内,作为生物医药创新领域的前沿,RNA干扰药物已经被列入到《"十三五"生物产业发展规划》重点发展领域。
目前,国内siRNA 在研药物进展最快的当属视神经保护的创新药物 QPI-1007。该在研药物是一种人工合成的 siRNA,由苏州瑞博生物与美国Quark制药共同开发,按照合作协议,苏州瑞博生物拥有该药物在中国及亚洲(少数特定国家除外)的开发和市场权益。
QPI-1007通过暂时抑制促凋亡蛋白半胱天冬酶 2 的表达拟实现用于非动脉炎性前部缺血性视神经病变(NAION)的治疗,同时具有青光眼的治疗潜力。QPI-1007 的全球关键性 II/III 临床研究 QRK207,是针NAION的国际多中心临床试验,目前已在国内完成了首例受试者给药,该项临床研究是在我国进行的首个 siRNA 药物临床试验,具有里程碑时的意义。
来源:新浪医药
版权及免责声明:本网站所有文章除标明原创外,均来自网络。登载本文的目的为传播行业信息,内容仅供参考,如有侵权请联系答魔删除。文章版权归原作者及原出处所有。本网拥有对此声明的最终解释权。


{replyUser1} 回复 {replyUser2}:{content}