发现新机制!攻克黑色素瘤耐药性又近一步
靶向疗法是针对黑色素瘤的一种有效治疗方案。其中,BRAF抑制剂和MEK抑制剂的组合疗法已得到广泛应用,可惜的是,一些患者会对治疗产生获得性耐药。近日,美国费城的Thomas Jefferson University的科学家们发现,BRAF上的一个位点对获得性耐药有影响,他们希望这一发现能导致更好的组合疗法问世。研究论文发表在《Cell Reports》上。
黑色素瘤是皮肤肿瘤中最致命的类型,特别是晚期黑色素瘤有较高的转移风险。对于已发生转移的黑色素瘤患者,即使接受手术治疗,患者仍有较高复发风险,因为术后仍可能有黑色素瘤细胞残留在体内。数据显示,如果术后不继续接受辅助治疗,接近一半(41%)的患者会在第一年内复发疾病。辅助治疗是在手术切除肿瘤后进行的额外治疗,通常推荐给高风险黑色素瘤患者使用以降低复发风险。用于进行辅助治疗的药物常是靶向黑色素瘤的癌驱动基因(比如BRAF)。
全世界每年约有20万名新的黑色素瘤患者确诊,其中约一半患者具有BRAF突变。BRAF是处于RAS/RAF/MEK/ERK通路中的丝氨酸/苏氨酸激酶,其细胞信号通路中的蛋白大多具有促进细胞生长和存活的功能,如果它们发生突变,就有可能引起细胞无限制的增殖,最终发展成癌症。靶向这些蛋白的抑制剂药物能关闭它们的激酶功能,从而起到遏制肿瘤生长的目的。同时使用针对两个目标的抑制剂,有可能降低肿瘤细胞发展出耐药性的几率,达到更好的抗癌效果。因此,有多种获得FDA批准的治疗方案是针对BRAF V600E突变以及下游的MEK蛋白,包括诺华的Tafinlar和Mekinist,罗氏的Zelboraf和Cotellic,以及Array BioPharma的Braftovi和Mektovi等。然而,患者中约有13% - 30%的人携带有异常剪接版本的BRAF V600E,他们即使接受BRAF-MEK抑制剂的组合疗法,病情也依然会发展。
以前的研究认为,BRAF与其底物MEK之间的接触增加是导致耐药性的原因,但具体原因仍待阐明。这项新研究的结果帮助研究者进一步理解这一机制:RAF激酶能磷酸化并激活MEK,调控细胞增殖的信号途径。在耐药性黑色素瘤中,BRAF蛋白能与MEK蛋白发生二聚化(dimerization),之间的结合力增加,导致信号异常持续激活,并不受药物抑制的调控。研究者试图鉴定是什么导致了异常剪接版本的BRAF V600E与MEK的结合力增加,他们发现,位于BRAF磷酸结合部位的丝氨酸729(S729)可能起了重要作用。
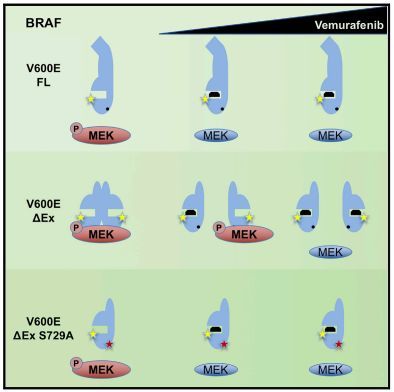
▲丝氨酸729可能导致了异常剪接版本的BRAF V600E与MEK的结合力增加(图片来源:《Cell Reports》)
研究结果显示,在耐药性患者中,RAF抑制剂能增加S729的磷酸化。如果将S729突变成无法被磷酸化的状态,就能阻断RAF与MEK的结合,减少二聚化复合物的形成,并且还能恢复BRAF抑制剂的效力。同理,在BRAF二聚化位置导入突变也能影响其与MEK的结合,增加RAF抑制剂的效果。因此,研究者认为BRAF S729对RAF抑制剂耐药起重要作用,应该进行更多研究来了解S729如何直接或间接地促进BRAF与MEK的作用。
“这项工作有助于解释RAF抑制剂耐药性的双重假设,其中一个侧重于MEK,另一个侧重于二聚化,”该研究的主要作者Andrew Aplin博士表示:“这项工作将两者的机制贯通起来,结果可能有助于设计更好的黑色素瘤组合疗法。虽然破坏BRAF二聚化与临床前模型中的有利结果相关,但要广泛应用这类策略,还需要直接测试这种治疗会如何影响蛋白质与其底物结合的效果。”
参考资料:
New BRAF insight sheds light on strategy against drug-resistant melanoma
来源:新浪医药
版权及免责声明:本网站所有文章除标明原创外,均来自网络。登载本文的目的为传播行业信息,内容仅供参考,如有侵权请联系答魔删除。文章版权归原作者及原出处所有。本网拥有对此声明的最终解释权。


{replyUser1} 回复 {replyUser2}:{content}