Camurus公司Buvidal获欧盟批准 系首个阿片依赖长效治疗药物

Camurus是一家瑞典制药公司,致力于开发和商业化用于治疗严重和慢性疾病的创新差异化药物。近日,该公司宣布,欧盟委员会(EC)已批准每周一次和每月一次的Buvidal(长效丁丙诺啡,CAM2038),用于16岁及以上青少年和成人治疗阿片依赖。此次批准,使Buvidal成为欧盟获批治疗阿片依赖的首个长效药物。Camurus公司已计划在2019年第一季度将Buvidal推向首批欧洲国家。
Buvidal是一款可每周和每月使用一次的丁丙诺啡长效皮下注射剂,采用Camurus公司专有的流体结晶(FluidCrystal)注射积存(injection depot)技术开发。Buvidal是一种溶解有丁丙诺啡的脂质基液体,一旦注射皮下,当注射液与皮肤组织中的液体接触时,脂质基液体会转变为结晶凝胶,形成凝胶样积存库,该积存库随时间缓慢生物降解,释放丁丙诺啡。丁丙诺啡可阻断阿片类药物在大脑中的成瘾作用,减少戒断症状、阿片渴求以及非法阿片类药物的使用。
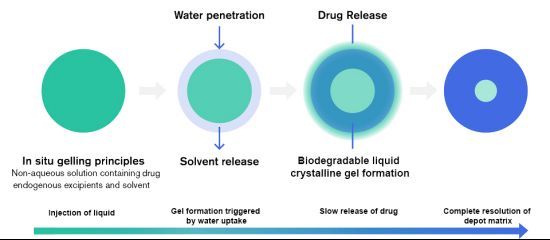
流体结晶注射积存技术(来源:Camurus公司网站)
英国伦敦国王学院国家成瘾中心主任Sir John Strang教授表示,“欧洲的阿片依赖患者非常需要能够改善治疗效果和生活质量的新的、更有效的药物。Buvidal通过每周一次或每月一次皮下注射给药,可显著改善依从性并减少日常治疗负担,该药将为阿片依赖治疗领域带来一场革命。”
Camurus公司总裁兼首席执行官Fredrik Tiberg博士表示,“欧盟委员会批准Buvidal,将为欧洲50多万阿片依赖患者提供一种创新和急需的新治疗方案,目前这类患者正在接受每日一次的药物治疗。Buvidal的获批对公司而言是一个重要里程碑,该药是验证了我们流体结晶技术的第一个长效药物。”
欧盟委员会批准Buvidal是基于一个全面的全球开发项目的安全性和有效性数据。该项目有7个临床研究,包括入组了428例阿片依赖患者的随机、双盲、双模拟、阳性对照III期研究。该研究表明,与每日一次的标准治疗药物丁丙诺啡/纳洛酮舌下片相比,Buvidal提供了更好的治疗效果。
目前,Buvidal也正在接受澳大利亚和美国的监管审查。美国方面,FDA已向Camurus的美国合作伙伴Braeburn指定了Buvidal的PDUFA目标日期为2018年12月26日。
来源:新浪医药
版权及免责声明:本网站所有文章除标明原创外,均来自网络。登载本文的目的为传播行业信息,内容仅供参考,如有侵权请联系答魔删除。文章版权归原作者及原出处所有。本网拥有对此声明的最终解释权。


{replyUser1} 回复 {replyUser2}:{content}