2019年,这15个临床试验值得关注!

刚刚过去的2018年,是创新疗法层出不穷的一年。这一年里,我们看到了首款RNAi疗法的诞生,也见证了又一款“不限癌症”的广谱抗癌药获批。在今年,哪些创新药将迎来关键临床结果?又有哪些创新疗法有望取得重要的进展?新年到来之际,结合Xconomy的盘点内容,为大家送上今年十五大值得关注的临床试验。
临床试验:ENGAGE,EMERGE
疾病领域:阿兹海默病
研发公司:Biogen(渤健)
阿兹海默病是困扰全球的一大疾病。据估计,到2050年,仅在美国,就将有1400万人生活在阿兹海默病的阴影之下。作为全球第六大死因,阿兹海默病每年造成了数十亿美元的医疗支出。

在这两项临床试验中,研究人员们专注的新药叫做aducanumab,它基于的是“淀粉样蛋白假说”。尽管之前所有针对这一靶点的新药都在临床试验中折戟沉沙,但Biogen的研究人员们依然决定推进这一疗法的研发。他们希望能够通过预防淀粉样蛋白的沉积,起到改善认知和运动能力的效果。
2017年,在一项大型的1期临床试验中,研究人员们看到了积极的迹象。他们发现,随着剂量的上升,患者脑中的淀粉样蛋白沉积随之下降。以此为基点,研究人员们决定启动两项大型的3期临床试验ENGAGE与EMERGE。而他们要挑战的是一座险峰——证实药物对认知能力有改善,且不会有危险的副作用。

▲这款新药的早期临床结果曾登上《自然》封面(图片来源:《自然》)
去年2月,Biogen宣布将招募额外500名患者进行评估,让人们一度对这两项研究的前景产生了担忧。而由于患者招募规模的扩大,这两项研究的结果可能要到2019年末,乃至2020年才会得到揭晓。无论结果如何,这款新药的成绩都会在业内带来重要的影响。
临床试验:NCT03375164(Sarepta)、IGNITE-DMD(Solid Bio)、NCT03362502(辉瑞)
疾病领域:杜氏肌营养不良症
研发公司:见上
这几年来,我们在杜氏肌营养不良症的治疗上取得了诸多突破,也迎来了美国FDA批准的首款疗法Exondys 51(eteplirsen)。然而,这些突破并没有改变该疾病依然致命的事实。

在全球范围内,有大约30万名男孩受这种疾病的影响。由于肺部或心脏问题,他们往往会在年纪轻轻的时候,就不幸去世。类固醇药物和eteplirsen的确可以缓解进程,但无法改变结局。
这正是基因疗法有望展现身手的地方。这里的三家公司都将在2019年公布临床数据,而这些公司开发的疗法,是通过改造病毒,将微肌营养不良蛋白(micro-dystrophin)递送到患者体内,弥补患者的缺失。如果一切顺利,一次输注后,患者就能长期产生这些蛋白,起到治疗疾病的效果。
与对照组相比,基因疗法能否显著改善患者的运动能力?2019年,这个问题的答案有望变得更加清晰。
临床试验:Gener8-1
疾病领域:甲型血友病
研发公司:BioMarin Pharmaceutical
这又是一项关于基因疗法的研究。在这项3期临床试验里,来自BioMarin的研究人员们将评估valoctocogene roxaparvovec对于患者的治疗效果。按计划,该试验将在今年第二季度完成招募。如果一切顺利,这款基因疗法有望随后向美国FDA递交上市申请。

这将改变血友病治疗的格局。先前,血友病患者需要频繁注射凝血因子,帮助凝血。但频繁的治疗给患者带来了不便,有时凝血因子的不足也不能完全杜绝出血的发生。此外,这种疗法的开销每年在25万到40万美元左右,价格不菲。
在BioMarin之外,UniQure,辉瑞,以及Spark Therapeutics也在开发治疗血友病的基因疗法。我们相信,距离首款血友病基因疗法的问世,已经不远了。
临床试验:KarMMA,NCT02514239
疾病领域:多发性骨髓瘤
研发公司:新基/bluebird bio;安进(Amgen)
免疫疗法已经彻底改变了许多癌症的治疗格局,而多发性骨髓瘤可能就是下一个得到革命性治疗的癌症类型。目前,许多公司正在开发靶向BCMA的CAR-T疗法。这种蛋白在骨髓内的致癌性B细胞上大量表达。通过靶向这些表达BCMA蛋白的细胞,我们有望改变血液癌症的治疗。
目前,我们在早期临床试验中看到了一些积极的成果,患者也取得了很好的缓解率。然而,研究人员们尚有一些问题有待解决,这包括了这些疗法的持续时间,以及它们能够治疗的患者群体有多大。

有些问题将在2019年得到解答。其中,bb2121的KarMMA临床数据将得到公布。新基与合作伙伴bluebird bio带来的这款疗法,在一切顺利的情况下,有望在2020年得到批准。而他们带来的一款改良过的疗法bb21217也已进入研发跑道。除此之外,南京传奇/强生,以及Poseida Therapeutics等公司带来的疗法,也正在快速研发之中。
值得一提的是,靶向BCMA的未必仅仅是CAR-T疗法。安进的AMG-420作为一款抗体药物,能够同时靶向T细胞和BCMA,从而将T细胞带到癌细胞附近,促进杀伤。目前,这款疗法的1期临床试验结果刚刚得到公布。更多数据将在2019年揭晓。
临床试验:PIVOT-2
疾病领域:实体肿瘤
研发公司:百时美施贵宝(BMS),Nektar Therapeutics
2018年,BMS宣布与Nektar达成合作,计划将后者的NKTR-214与Opdivo联用,测试对于实体肿瘤的治疗效果。这也是截止至目前,最引人关注的免疫组合疗法之一。

和其他免疫检查点抑制剂一样,Opdivo对不少癌症有着极佳的治疗效果,但能从中受益的患者比例却不在多数。为此,诸多医药公司正在着力开发组合疗法,以求对更多患者进行治疗。在IDO抑制剂出师不利后,NKTR-214进入了人们的视野。作为一款IL-2(CD122)激动剂,它有望增强免疫系统的活性。但人们也需要注意激活的“度”,避免产生危险的副作用。
在3期临床试验中,研究人员们将专注于黑色素瘤和肾癌。去年11月,初期的临床数据并不乐观。至于最终分析结果如何,还需要等待今年的更多信息。
临床试验:NCT03066258
疾病领域:年龄相关性黄斑变性
研发公司:RegenxBio
年龄相关性黄斑变性是最常见的失明原因之一。在美国,它大约影响了200万名患者。到2050年,这一数字将达到550万人,翻倍还有余。
湿性年龄相关性黄斑变性(wAMD)是这种疾病里,较为严重的类型。为了治疗这一疾病,患者必须定期往眼睛里注射药物,治疗不便,且成本不菲。不少医药公司将注意力放在了注射次数更少的药物上,而RegenxBio则试图一劳永逸,通过RGX-314这款基因疗法,在患者眼睛里表达抑制VEGF的蛋白质,一次治疗,长期生效。

但这一疗法的前方并非都是坦途。事实上,之前也有不少人尝试开发针对这一疾病的基因疗法,但结果并不顺利。有人指出,RGX-314也有不少局限,比如它必须注射在眼睛的多个不同部位,手术存在风险。此外,目前的疗法虽然繁琐,但很有效,因此基因疗法需要很好定义自己如何才算成功。第三,基因疗法并不能降低治疗成本。
但一个利好消息在于,2017年,我们已经有了一款治疗眼部疾病的基因疗法获批上市。从监管上看,这是一个积极的信号。此外,1期临床试验结果的数据也同样喜人。
临床试验:L-MIND,B-MIND
疾病领域:弥漫性大B细胞淋巴瘤
研发公司:MorphoSys
弥漫性大B细胞淋巴瘤(DLBCL)是最常见的非霍奇金淋巴瘤。目前获批的两款CAR-T疗法,针对的也正是这一疾病。从治疗流程上看,新诊断的患者会先接受Rituxan/化疗的组合疗法。如果这一疗法不再起效,患者就需要接受高剂量的化疗、干细胞移植、或是CAR-T疗法。

MorphoSys则带来了一种全新的选择。其在研疗法MOR208是一种靶向CD19的抗体。在一项2期临床试验中,MOR208与lenalidomide的组合,能在经治的患者中,阻止疾病的扩散,中位数达到16个月以上。一些专家表示,这是在这一患者群体中“前所未有的发现”。如果后期研发顺利,这款新药有望在2020年获批。而关键的临床结果,则将在2019年揭晓。
临床试验:NCT02978326;NCT03672175
疾病领域:产后抑郁症 / 重度抑郁症
研发公司:Sage Therapeutics
抑郁症是一种流行病。仅在美国,就有超过1800万人罹患重度抑郁症。此外,有14%的女性在生育后会受抑郁症的影响。在发达国家,产后抑郁是生育后,母亲死亡的最常见原因。

无论是重度抑郁症,还是产后抑郁症,背后的核心都是一致的。因此,Sage正在研发SAGE-217,治疗这两种疾病。作为一款靶向GABA的药物,它有望缓解抑郁的症状。事实上,Sage的brexanolone具有同样的机理,并有望在今年3月获批。与brexanolone不同,SAGE-217是一种药片,无需像brexanolone那样,对患者进行连续输注。它能否取得成功,我们拭目以待。
临床试验:REGENERATE,RESOLVE-IT
疾病领域:非酒精性脂肪性肝炎(NASH)
研发公司:Intercept Pharmaceuticals, Genfit
有些疾病是可以预防的,但是只靠预防可能不会对患者产生多大的影响。这方面的范例就是不良饮食和锻炼习惯而导致的脂肪肝。有些脂肪肝会进一步恶化成为非酒精性脂肪性肝炎(NASH),患者肝脏会出现炎症,肝硬化和瘢痕组织。NASH可能导致肝癌,在美国也是导致每年数千例肝脏移植手术的原因。NASH已经成为全球性疾病。
目前没有获得FDA批准治疗NASH的疗法,因此多家公司争先进入这一领域开发可改变疾病进程的疗法。目前位于纽约的Intercept Pharmaceuticals和法国公司Genfit的在研疗法已经进入临床后期。Intercept公司应该是第一个汇报3期临床数据的公司,该公司的奥贝胆酸片(obeticholic acid)已经获得FDA批准治疗一种与NASH相关的罕见肝病。

在包含2370名患者的REGENERATE临床试验中,Intercept期待奥贝胆酸片在使用18个月后能够减少肝脏疤痕组织的产生或者降低一系列预先设定的与疾病相关的症状。更广泛地说,Intercept希望通过比较治疗组和对照组患者的死亡率,住院率,癌症发生几率等数据,来证明这一疗法能够长期改善患者的预后状况。理想情况下,NASH的疗法能够减少这一疾病的三个标志性症状,肝脏纤维化,炎症和肝脏脂肪水平。
Genfit包含2000名患者的RESOLVE-IT的3期临床试验数据将在今年晚些时候公布。这一试验的主要目标是NASH症状消除。

除了这两家公司以外,多家生物医药公司拥有不同的NASH候选药物。它们包括吉利德科学(Gilead Sciences),艾尔建(Allergan),诺华(Novartis),NGM Biopharmaceuticals,默沙东(MSD),Madrigal Pharmaceuticals,Viking Therapeutics,罗氏(Roche),辉瑞(Pfizer),百时美施贵宝(BMS),89Bio,和Akero Therapeutics等等。这一领域具有重大医疗需求,可以预见,NASH领域今后仍将是研发活动非常活跃的疾病领域。
临床试验:NCT03745287, NCT03041324
疾病领域:罕见遗传病
研发公司:CRISPR Therapeutics, Editas Medicine, Sangamo Biosciences
在2017年末,第一款编辑基因组的疗法开始了临床试验。Sangamo Biosciences公司治疗罕见遗传病II型粘多糖贮积症(MPS II)的SB-913使用锌指核酸酶(ZFN)基因组编辑技术,将正确的基因插入到肝细胞基因组里的特定位点。MPS II患者由于遗传原因导致体内特定蛋白酶缺乏,造成骨骼和器官异常和认知问题。大多数患者无法活过青春期,目前对这种疾病的治疗方法是每周向患者注射他们体内缺乏的蛋白酶。

基因编辑可以让患者的细胞重新开始生成缺失的蛋白酶,它可能为患者提供一个长期的解决办法。基因编辑疗法的疗效到底能够持续多久,是基因组编辑时代任何疗法都需要回答的最重要的问题之一。
在2019年,我们可能获得第一个CRISPR人类临床试验的结果。CRISPR Therapeutics和Editas Medicine公司都启动了CRISPR的临床试验。

CRISPR Therapeutics和Vertex Pharmaceuticals公司治疗镰状细胞贫血症(SCD)的1/2期临床试验将包括大约45名严重SCD患者。名为CTX001的疗法将获取患者的造血干细胞,通过基因编辑提高它们生成胚胎血红蛋白的能力,然后将经过基因编辑改造过的细胞输回患者体内。
而由知名学者张锋创建的Editas Medicine公司将启动治疗Leber先天性黑朦10型的临床试验,将名为EDIT-101的CRISPR疗法直接注射到10到20名患者的视网膜中,力图在视网膜的感光细胞中删除造成疾病的基因突变。

这两项CRISPR临床试验都不会将CRISPR疗法注射到血循环中,因此可能帮助降低基于CRISPR疗法的潜在风险。然而只有临床试验结果才能最终揭示这些疗法的潜在风险,这也是这些临床试验值得关注的原因。
临床试验:ORION-9, ORION-10, ORION-11
疾病领域:心血管疾病
研发公司:The Medicines Co./Alnylam Pharmaceuticals
在2015年,一类称为PCSK9抑制剂的创新降低胆固醇新药获得批准。它们可以大幅度降低“坏”胆固醇——LDL-C,为那些对他汀类药物反应不佳或者使用他汀类药物后仍然需要进一步降低胆固醇水平的患者提供了一项创新选择。

The Medicines Co.和Alnylam Pharmaceuticals合作开发的inclisiran可能进一步降低这类疗法的成本。Inclisiran是一种RNAi疗法,它通过利用RNA干扰技术,防止肝脏生成PCSK9蛋白。与已有PCSK9抑制剂相比,这一疗法的一个重要优势是患者只需每年接受2-3次注射就可以达到控制胆固醇水平的效果,而已有PCSK9抑制剂需要每月接受一到两次注射。
在ORION-9,ORION-10和ORION-11临床试验中,心血管疾病患者将在18个月中接受4剂inclisiran或者安慰剂的治疗。试验数据预计在2019年下半年公布,如果试验数据积极,The Medicines Co.预计将在2019年年底递交新药申请。
这些ORION临床研究同时是在广泛人群中使用RNAi疗法的第一组大型试验,它的结果可能预示RNAi疗法作为一种治疗疾病的新模式,能够在更广泛的领域得到应用。
临床试验:STRONG/SPR1NT(诺华), FIREFISH/SUNFISH(罗氏)
疾病领域:脊髓肌肉萎缩症(SMA)
研发公司:诺华,罗氏
对于罕见遗传病SMA的患者来说,他们能够选择的疗法在过去几年出现了重大转变,这一转变在2019有望进一步加快。
SMA患者由于脊髓中的运动神经元退化,导致无法行使基本运动功能。在2016年,FDA批准了渤健(Biogen)和Ionis Pharmaceuticals联合开发的nusinersen反义寡核苷酸(ASO)疗法。这款疗法能够在多种类型的SMA患者中延缓疾病进程。而在今年,多款基因疗法和口服疗法可能问世。
诺华与AveXis共同开发的基因疗法AVXS-101(Zolgensma)在去年已经获得FDA授予的优先审评资格,用于治疗1型SMA患者。今年,诺华期望这款疗法能够在其它类型的SMA患者中表现出疗效。治疗2型SMA患者的STRONG临床试验和治疗1,2,3型未显示出症状的SMA患者的SPR1NT临床研究预计在今年5月前公布结果。

罗氏与PTC Therapeutics公司合作开发的risdiplam是一种提高运动神经元生存(SMN)蛋白水平的口服疗法。治疗1型SMA患者的FIREFISH和治疗2,3型患者的SUNFISH临床试验预计今年将汇报结果。如果结果积极,罗氏可能在2020年向FDA递交新药申请。

临床试验:HOPE(Part A)
疾病领域:镰状细胞贫血症(SCD)
研发公司:Global Blood Therapeutics
虽然基因疗法最终可能一劳永逸地纠正SCD患者体内导致疾病的基因突变,但是这些基因疗法可能还需要数年才能成功上市。同时,世界上有上百万SCD患者需要治疗。SCD患者的血红细胞会变形并且阻塞血管,患者可能出现疼痛危机并且出现中风、器官衰竭,甚至早夭。

最接近上市的潜在新药是Global Blood Therapeutics(GBT)公司的voxelotor。这是一种口服疗法,能够增强血红蛋白与氧气的结合能力,从而防止血红蛋白聚集和血红细胞变形。GBT公司进行的HOPE临床试验的中期数据表明,voxelotor与安慰剂相比,能够显著提高患者的血红蛋白水平。而且,FDA已经允许GBT公司使用加速批准途径提交新药申请,这意味着该公司可以使用替代终点衡量voxelotor的疗效。
在2019年,GBT公司将进一步更新HOPE试验的结果,提供从更多患者中获得的数据。更全面的结果将帮助衡量voxelotor的疗效和安全性。
临床试验:NCT03525548, NCT03525444
疾病领域:囊性纤维化(CF)
研发公司:Vertex Pharmaceuticals
Vertex公司已有的药物能够为40%的CF患者改变疾病进程。而今年公布的试验数据将指明该公司开发的组合疗法能否造福高达90%的CF患者。

该公司在两项3期临床试验中检测VX-659/ivacaftor/tezacaftor和VX-445/ivacaftor/tezacaftor两组组合疗法的疗效。VX-659/ivacaftor/tezacaftor的组合疗法已经达到了临床试验的主要终点。另一组组合疗法的试验结果预计在今年第一季度公布。Vertex计划在今年年中选择表现更好的一组组合疗法向FDA递交新药申请。
临床试验:NCT03313778, NCT03370887, NCT03313778, NCT03392389
疾病领域:癌症/传染病
研发公司:Moderna
致力于开发mRNA疗法的生物医药公司Moderna在融资和IPO方面创下了多项纪录。而今年该公司公布的临床试验结果将向人们展示该公司mRNA疗法的治疗潜力。


Moderna公司有10款候选药物在临床试验中接受检验,其中包括传染病或癌症疫苗。有些试验在今年将第一次公布试验数据。而该公司与阿斯利康(AstraZeneca)合作开发的AZD8601预计将在2020年公布2期临床结果,这是该公司唯一一个进入2期临床试验的研发项目。AZD8601是一种编码VEGF-A的合成mRNA分子,它可能帮助心血管疾病患者改善血液流通,辅助心脏组织再生。
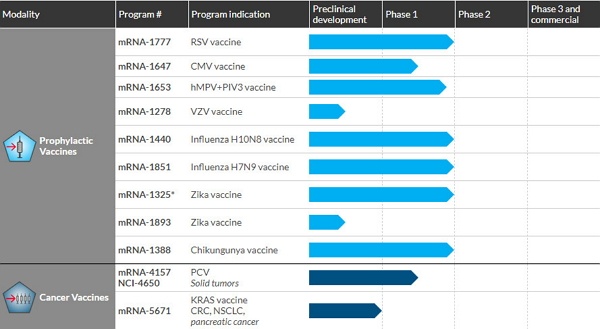
▲Moderna公司预防性疫苗和癌症疫苗方向的研发管线(图片来源:Moderna官方网站)
今年其它mRNA公司也将公布早期临床数据,这些数据将为这一新治疗模式提供初步证据。Translate Bio公司治疗囊性纤维化的1/2期临床试验正在进行中,中期数据预计在2019年中公布。CureVac公司正在进行两项1期试验,一项使用基于RNA的免疫疗法治疗实体瘤患者,另一项检验基于RNA的狂犬病毒疫苗。德国BioNTech公司今年可能公布两款肿瘤疫苗的1期临床结果,它们分别用于治疗黑色素瘤和三阴性乳腺癌。
我们预祝这些临床试验早日公布积极结果,为患者带来创新疗法。
参考资料:
[1] 15 for ’19: Key Clinical Data to Watch for Next Year (Part 1)
[2] 15 For ’19: Key Clinical Data to Watch For Next Year (Part 2)
来源:药明康德
版权及免责声明:本网站所有文章除标明原创外,均来自网络。登载本文的目的为传播行业信息,内容仅供参考,如有侵权请联系答魔删除。文章版权归原作者及原出处所有。本网拥有对此声明的最终解释权。


{replyUser1} 回复 {replyUser2}:{content}