科伦、复星、上药等企业8产品通过一致性评价 谁家竞争力强?

2018年结束的前几天,国家药监局放出重磅政策,业界一直担忧的一致性评价时限松动。
12月28日,国家药品监督管理局发布《关于仿制药质量和疗效一致性评价有关事项的公告》(以下简称《公告》)。《公告》披露,对已经纳入国家基本药物目录的仿制药品种,不再统一设置一致性评价时限要求。
政策并非无限期放宽,化学仿制药需要在首家品种通过一致性评价后3年内完成一致性评价。逾期未完成的,经申请认定后,方可予适当延期。
一致性评价时限虽有松动,但这一政策的延续没有动摇。
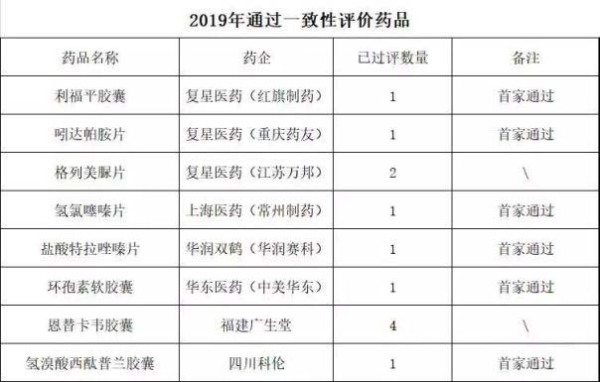
1、复星医药已有12产品过评
在一致性评价投入方面,复星医药成绩相对亮眼,至少已有12个产品过评。
复星医药在大健康产业内布局甚广,不仅在最近非常火热的生物创新药上大量投入,而且在医院、互联网医疗、医药商业流通、医疗器械等领域加大布局,在全球建立研发体系。但其对仿制药的投入也不低,根据复星医药2018年半年报,当期内在进行的一致性评价项目共有55个。
复星医药2019年最先过评的3个药物在市场份额、市场容量方面处于完全不同的情形。
利福平胶囊是复星医药旗下红旗制药的产品。该产品在2018年还未有销售额,根据IQVIA数据,2017年度利福平制剂于中国境内销售额约为人民币3.2亿元。目前国内共有450家企业生产,为289品种、医保目录药品,红旗制药为首个通过一致性评价的,此外,杭州民生药业也在申请一致性评价中。
而另一过评药为复星旗下江苏万邦的格列美脲片,该药品适用于控制饮食、运动疗法及减轻体重均不能充分控制血糖的2型糖尿病。2017年度,江苏万邦该药品于中国境内销售额约为人民币2.4亿元,而根据IQVIA数据,2017年度格列美脲片于中国境内销售额约为人民币9.7亿元,复星的市场份额相对较大,而该药目前通过一致性评价的仅有扬子江,但还在申请中的还有6家。
吲达帕胺片是复星今年通过的第三个品种,为289目录、国家医保目录药品。该药品主要用于治疗原发性高血压。2017年度,复星旗下重庆药友该药品于中国境内销售额约为人民币145万元。根据IQVIA最新数据,2017年度吲达帕胺片于中国境内销售额约为人民币6,918万元,复星的份额相对较小,其虽为首个过评,但目前还有10家正在申请中。
2、科伦重兵布局抗抑郁领域
1月25日,科伦药业发布公告,公司一款抑郁症治疗药物通过仿制药质量和疗效一致性评价,为国内首家通过的相关产品,该药物即氢溴酸西酞普兰胶囊,通过一致性评价的同时获得药品注册批件。
科伦药业股份有限公司是一家专注于医药输液行业的企业。
此前,科伦药业已有两款抑郁症治疗药物通过一致性评价,并且为国内首家通过的产品。其中一款药品就是草酸艾司西酞普兰片,2016年草酸艾司西酞普兰片中国销售额约12.5亿元人民币,位居抗抑郁类药物首位。
氢溴酸西酞普兰片也是继草酸艾司西酞普兰片之后,科伦第二个首家通过一致性评价治疗抑郁症的品种。
氢溴酸西酞普兰片为新型抗抑郁药中耐受性最佳的药物之一,是国内外权威指南推荐的一线抗抑郁药,也被纳入国家医保乙类,据科伦公告称,2017年该药中国销售额约3.04亿元人民币。
此次过评的氢溴酸西酞普兰胶囊使得科伦药业在抑郁症药物上又再得以扩展和加强。
3、乙肝大药恩替卡韦又有一家过评
2019 年,广生堂恩替卡韦胶囊通过仿制药质量与疗效一致性评价。至此,该公司两大主力产品恩替卡韦胶囊和替诺福韦胶囊作为慢性乙型肝炎防治指南一致推荐的一线药物,均顺利通过一致性评价。
其中,恩替卡韦在我国目前核苷(酸)类抗乙肝病毒市场占有率位居第一,替诺福韦是近两年中国增速最快的抗乙肝病毒药物。该两大产品均被列入国家医保目录。
据统计预测,2020 年我国治疗乙肝用药的市场规模将达到200亿元,复合年均增长率超过 20%。
恩替卡韦2017年在中国公立医疗机构终端销售额为84.25亿元,同比增长8.59%,市场领军企业正大天晴占比47.29%,施贵宝占比34.46%。
恩替卡韦同时也是4+7带量采购中极富争议的品种,正大天晴的恩替卡韦分散片在带量采购中以17.36元/盒的价格中选,降幅达到96%。目前恩替卡韦通过仿制药一致性评价的企业已达6家,市场竞争激烈。
截至2019年1月18日,全国通过(或视同通过)一致性评价的品规数为173个,涉及产品87个。截至2018年底,289目录中通过一致性评价药品的仅有22个,完成度为7.61%。
未来,伴随国家药品集中采购试点等工作的推进,一致性评价将不仅是衡量和保证仿制药质量的门槛,还将对品种后续的市场份额带来巨大影响,显然2019年,一致性评价工作将继续成为众多药企的重点推进项目。
来源:新浪医药
版权及免责声明:本网站所有文章除标明原创外,均来自网络。登载本文的目的为传播行业信息,内容仅供参考,如有侵权请联系答魔删除。文章版权归原作者及原出处所有。本网拥有对此声明的最终解释权。


{replyUser1} 回复 {replyUser2}:{content}