新适应症国内获批 全球首款PCSK9抑制剂借力提升业绩
作者:小药丸
近日,安进旗下PCSK9抑制剂Evolocumab(依洛尤单抗,瑞百安/Repatha)第二个适应症在国内获批,用于成人动脉粥样硬化性心血管疾病的治疗,以降低心肌梗死、卒中和冠状动脉血运重建的风险,该药物成为中国首个获批用于心血管事件风险降低的PCSK9抑制剂。
在华获批的首款PCSK9抑制剂
安进Repatha已经于2018年7月31日获得国家药品监督管理局批准,用于成人或12岁以上青少年的纯合子型家族性高胆固醇血症,这是首个在华获批的PCSK9抑制剂。
2015年7月,Repatha在欧盟批准,成为全球首款获批上市的PCSK9抑制剂,随后8月Repatha又获得了FDA批准。
除了安进的Repatha之外,目前全球已获批的PCSK9抑制剂还有赛诺菲的Praluent。值得一提的是,在美国市场PCSK9新药开发竞赛中,赛诺菲使用了一张价格为6750万美元的加速审评券,将Praluent的审查周期缩短了4个月,最终Praluent领先Repatha一个月的时间率先获得了FDA的批准。
2017年12月,Repatha的新适应症申请获得了FDA的批准,此次批准使得Repatha成为全球第一款可用于预防心血管疾病成年患者心脏病、中风以及冠状动脉重建术的PCSK9抑制剂。
Repatha上市后业绩乏善可陈
在体内,低密度脂蛋白胆固醇(LDL-C)是公认的心血管疾病的主要风险因子。PCSK9蛋白可降低肝脏从血液中清除LDL-C的能力,通过抑制这种蛋白靶标的生物学活性,PCSK9抑制剂为对抗LDL-C提供了一种全新的治疗模式。这类药物也因此被视为继他汀类之后降脂药物领域的最大进步,业界对这类药物的表现寄予了厚望。
早在PCSK9抑制剂这类药物上市之前,RBC Capital Markets的分析师预计这类药物的市场将超过90亿美元,即使是大多数人相对保守的估计,这类药物的年度销售额也高达30亿美元。
2015年获批之后,Repatha的销售额为1000万美元,2016、2017年的全球销售额分别为1.41亿美元和3.19亿美元。这种表现显然与先前业内人士对PCSK9这类新型降脂药物的预期表现相去甚远,同时对照多数重磅炸弹级药物上市之后的早期表现,Repatha上市后的业绩表现确实乏善可陈。
新适应症加持&全系产品降价出售
Repatha未来表现有待考验
2017年12月,Repatha新适应症获得FDA批准,这为Repatha带来了新的市场机会。
2018年第一季度,Repatha创造了1.23亿美元的销售额,上年同期仅有9800万美元。第二季度延续了第一季度的增长态势,该季度的销售额达到1.48亿美元,2018上半年同比增长105.3%。
此次,上述新适应症在国内获批,这对于安进及国内的患者而言,都有着特殊的意义。根据中国2017年心血管报告,当前中国心血管疾病死亡率高于肿瘤及其他疾病,居于首位,占了我国居民疾病死亡构成的40%以上,预计未来10年心血管病患病人数仍将快速增长。国内广大心血管疾病患者需要更多新的治疗选择,同时拿下中国市场对于安进Repatha销售业绩的提升也别有意义。
从过去几年市场的反馈来看,Repatha销售业绩增长乏力的一个重要原因在于产品定价,尤其在上市初期,日均38.6美元折合年均大约1.41万美元的定价使Repatha遭受了来自消费市场的激烈抨击。
为了扩大Repatha在低收入人群中的可及性,2018年10月,安进将最常用的递送系统Repatha SureClick®autoinjector(自动注射器)在美国的定价下调至5850美元/年,比其最初14523美元/年的价格降低了大约60%。今年1月,安进宣布Repatha所有设备产品在美国市场均以目录价格60%的折扣出售,即每年5850美元,包括Repatha Pre-Filled Syringe(预充式注射器)、Repatha Pushtronex (带预灌装药筒的在体输注器)。
安进主动降价能够扭转颓势实现高速增长,依然有待时间的考验。同时面对着赛诺菲Praluent的市场竞争,Repatha在2024年实现Evaluate Pharma预计的42.6亿年度销售额,感觉依然很有压力。
本土制药企业进展概览
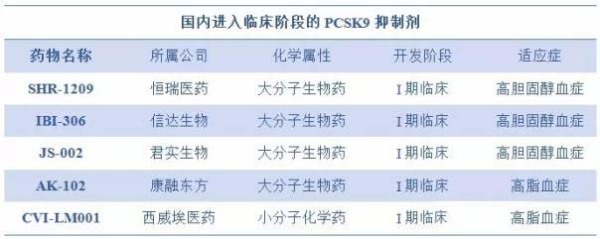
目前,国内已经有不少制药企业对PCSK9靶点进行了布局,其中恒瑞医药SHR-1209、信达生物IBI306、君实生物JS002、康融东方AK102及西威埃医药CVI-LM001已经进入了临床阶段。
不过,有了安进Repatha的前车之鉴,对于产品上市之后诸如销售业绩等问题,作为同类产品玩家的本土制药企业不妨提前好好思量一番。
来源:新浪医药
版权及免责声明:本网站所有文章除标明原创外,均来自网络。登载本文的目的为传播行业信息,内容仅供参考,如有侵权请联系答魔删除。文章版权归原作者及原出处所有。本网拥有对此声明的最终解释权。


{replyUser1} 回复 {replyUser2}:{content}