科学家发现载药“果冻”可剿灭伪装起来的肿瘤
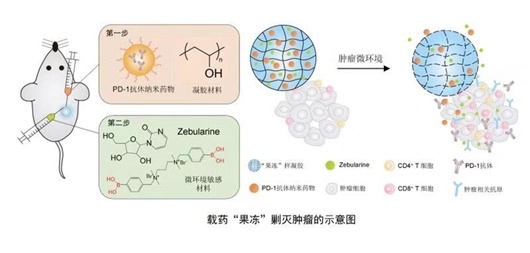
复旦大学药学院陆伟跃教授研究团队与加州大学洛杉矶分校顾臻教授研究团队合作研发出一种新型抗癌制剂,该制剂首先将体内T细胞上的一种蛋白(PD-1)抗体制备成纳米药物,与一种表观遗传药物一起混合进入该团队预先设计成功的生理响应型载药凝胶的溶液中,然后直接在瘤旁注射后形成半固体的“果冻”样凝胶,该凝胶能够在肿瘤微环境中缓慢降解,并逐渐释放药物,此联合给药可有效抑制癌细胞生长。
相关研究成果日前在线发表于《先进材料》,并作为封面文章重点介绍。
据悉,在肿瘤发生发展的过程中,表观遗传性质的改变(即基因的DNA序列虽无改变,但基因的功能却发生了遗传性变化,并最终导致表观的变化)对肿瘤细胞成功“掩人耳目”地逃避体内免疫系统的识别起着至关重要的作用。PD-1作为体内T细胞上的蛋白,能够识别其他细胞表面上的PD-L1蛋白,从而具有判断“敌友”的本领,也就是说,两种蛋白结合之后会向T细胞传递“我是自己人,别攻击我”的信号;但狡猾的癌细胞非常“聪明”,它也通过在自己的表面“涂上”PD-L1蛋白,伪装成正常细胞,来骗过T细胞的攻击,如同一只“披着PD-L1羊皮的狼”。
那么,如何能让这 “披着PD-L1羊皮的狼”暴露出真面目?研究人员通过使用PD-1的抑制剂,让免疫细胞擦亮眼睛,识别并攻击肿瘤, 同时又联用一种表观遗传药物(Zebularine,这是一种DNA去甲基化药物)来调控肿瘤细胞的表观遗传性,增强肿瘤相关抗原的表达,以促使其暴露真面目。研究人员发现,该表观遗传药物还能减轻肿瘤微环境抑制机体免疫应答的作用,增强免疫细胞对肿瘤的杀伤攻击作用。考虑到PD-1抗体抑制剂对正常机体也存在一定毒副作用,研究人员选择通过“局部给药,缓慢释放”的方法进行治疗。
“这项成果首先在皮下肿瘤动物模型中得到验证,不但肿瘤生长得到了显著的抑制,生存期也显著延长。”陆伟跃表示,研究人员通过建立多发性肿瘤模型,在一个瘤旁给予载药凝胶后,发现远端肿瘤的生长也得到了抑制,提示该治疗策略在多发性肿瘤治疗中也具有潜在临床应用价值。
“这为实现临床转化,研究团队将进一步在动物模型上评估制剂的安全性并优化有效性。” 顾臻说。
相关论文信息:


{replyUser1} 回复 {replyUser2}:{content}