盘点诺华即将在中国上市的7款产品
医药观澜/报道
据不完全统计,目前中国国家药品监督管理局(NMPA)正在办理来自诺华(Novartis)的10个上市申请受理号,涉及成分7种,其中4种尚未有同款在中国获批。这些产品大多数处于在审评审批中,若进展顺利,诺华有望在近期获得NMPA批准上市7款产品。另据GBI近日消息,诺华全球药物开发负责人兼首席医疗官John Tsai博士在接受《中国日报》采访时表示,鉴于NMPA已经加快新药审评审批速度,诺华预计在2023年前在中国提交50个新药申请。今天,我们提前了解一下这7款已在中国提交上市申请的产品。
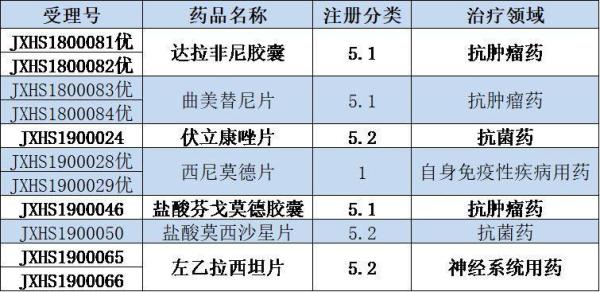
▲NMPA正在办理的10个上市申请受理号
1.芬戈莫德(fingolimod)
芬戈莫德是由诺华研发的一种新型免疫抑制剂,属于神经鞘氨醇1-磷酸受体调节剂,能促使淋巴细胞在淋巴结中滞留,达到抑制自身免疫反应的效果。2010年,该药获得美国FDA批准用于多发性硬化症(MS),2011年在欧洲获批用于复发缓解型多发性硬化症(RRMS)。
今年4月,NMPA药品审评中心受理了诺华芬戈莫德的上市申请。目前,该产品在NMPA的办理状态为在审批状态。多发性硬化症是以中枢神经系统蛋白质炎性脱髓鞘病变为主要特点的自身免疫病。芬戈莫德的获批,有望为MS患者带来新的治疗希望。
2.曲美替尼(trametinib)
曲美替尼是一种细胞外信号调节激酶抑制剂(MEK抑制剂),能够促进丝裂原活化,2013年被FDA批准用于治疗BRAF V600E/K突变不可切除或转移性黑色素瘤成人患者。2018年5月,FDA批准曲美替尼与达拉菲尼的组合,作为BRAF V600E/K突变黑色素瘤患者的辅助疗法。值得注意的是,这款组合疗法曾获得FDA突破性疗法认定和优先审评资格。
今年1月,药品审评中心受理了曲美替尼的上市申请,随后该药被纳入优先审评程序。目前,该产品在NMPA的办理状态为在审评审批中。黑色素瘤是中国发病率增长最快的恶性肿瘤之一,每年新发病例约2万例。曲美替尼的获批,将在一定程度上满足患者的临床需求。
3.达拉非尼(dabrafenib)
达拉非尼是一款BRAF抑制剂药物。该药不能用于野生型黑色素瘤,使用前需检测BRAF V600E突变。2013年,FDA批准了其用于治疗转移性黑色素瘤和不能行手术治疗的黑色素瘤病人。这是继维罗非尼、易普利单抗后,FDA批准的第三款治疗转移性黑色素瘤药物。
今年1月,药品审评中心受理了达拉非尼的上市申请,随后该药被纳入优先审评程序。目前,该产品在NMPA的办理状态为在审评审批中。

4.西尼莫德(siponimod)
西尼莫德是一种对S1P受体特定亚型具有高度选择性的S1P受体调控剂。它能够与淋巴细胞表面表达的S1P1受体亚型相结合,防止淋巴细胞进入多发性硬化症患者的中枢神经系统,从而降低炎症反应。今年3月,美国FDA宣布批准诺华开发的Mayzent(siponimod)上市,用于治疗复发型多发性硬化症成年患者。
在中国,药品审评中心于今年2月受理了西尼莫德的上市申请,随后该药被纳入优先审评程序。目前,该产品在NMPA的办理状态为在审评审批中。此前,多发性硬化症已被纳入中国《第一批罕见病目录》,西尼莫德的获批,有望为该患者群体带来新的治疗选择。
5.左乙拉西坦(levetiracetam)
左乙拉西坦属于吡咯烷酮类西坦类药物,最早于1999年以片剂形式在美国上市,缓释片剂型于2008年获FDA批准。癫痫是一种长期、慢性脑部疾病。在全球最畅销的抗癫痫药物中,作为广谱抗癫痫药的左乙拉西坦是抗癫痫药物市场领域的主力产品。
今年5月底,药品审评中心受理了诺华左乙拉西坦片的上市申请。目前,该产品在NMPA的办理状态为在审评审批中。数据显示,中国拥有近1000万癫痫患者,且每年新增病例数约为40万。目前,中国已有8款左乙拉西坦片国产药品获得注册批件。
6.伏立康唑(voriconazole)
伏立康唑是一种广谱的三唑类抗真菌药,是氟康唑的改进药,主要用于治疗侵袭性曲霉病、克柔念珠菌、足放线病菌属等真菌引起的感染。
今年2月,药品审评中心受理了诺华伏立康唑的上市申请。目前,该产品在NMPA的办理状态为在审评审批中。在中国,伏立康唑已有15款国产药品获得注册批件。
7.莫西沙星(moxifloxacin)
莫西沙星属于第四代喹诺酮类合成抗菌药,也是抗结核二线药品,适用于为治疗患有上呼吸道和下呼吸道感染的成人,如:急性窦炎、慢性支气管炎急性发作、社区获得性肺炎,以及皮肤和软组织感染。
今年4月,药品审评中心受理了诺华莫西沙星的上市申请。目前,该产品在NMPA的办理状态为在审评审批中。在中国,莫西沙星已有14款国产药品获得注册批件。
参考资料:
[1]国家药监局行政许可综合事项查询,Retrieved July 11, 2019 from http://sq.cfda.gov.cn/datasearch/schedule/search.jsp?tableId=43&tableName=TABLE43&columnName=COLUMN464,COLUMN475&title1=%E8%8D%AF%E5%93%81%E6%B3%A8%E5%86%8C%E8%BF%9B%E5%BA%A6%E6%9F%A5%E8%AF%A2
[2]诺华:计划2023年前在中国提交50个NDA,Retrieved July 10, 2019 from https://mp.weixin.qq.com/s?__biz=MzA5Njc0MTAxOQ==&mid=2649992879&idx=1&sn=102e95bb740ef40dec941e50a8799103&chksm=88ac7d5bbfdbf44d6153d138596011b965249f617a77e90614f515be0052e4cde1863131b8b0&mpshare=1&scene=1&srcid=0711p9jBtCBQz8m3yRUP82fb&pass_ticket=2OHE5g7Y0kfCNKCkZt3S2%2FmODmnwR9cLVR3IFCZqD10lykwtiUaM48JEFhA3XSMv#rd
来源:药明康德
版权及免责声明:本网站所有文章除标明原创外,均来自网络。登载本文的目的为传播行业信息,内容仅供参考,如有侵权请联系答魔删除。文章版权归原作者及原出处所有。本网拥有对此声明的最终解释权。


{replyUser1} 回复 {replyUser2}:{content}