NEJM:将存活率从8%提高到100%,基因治疗终迎来革命性突破
“这是最好的时代,这是最坏的时代;这是智慧的时代,这是愚蠢的时代……”对于基因治疗来说,现在的确是个最好的时代,已有多种基因疗法正式获批,为众多患者带来福音。
而对于不幸罹患遗传病的孩童们来说,基因疗法带来的,就是生与死的差别,至少对美国小姑娘Evelyn Villarreal是这样的。由于1型脊髓性肌萎缩症(SMA),Villarreal家的第一个女儿Josephine在1岁3个月大时就撒手人寰,Evelyn出生后不久也被确诊患上同样的疾病。脊髓性肌萎缩症是最常见也最致命的遗传病之一,即使进行治疗,绝大多数患儿也活不过20个月,Evelyn的父母绝望之情可想而知。
 Evelyn是个幸运儿,她已经可以和父母嬉戏了
Evelyn是个幸运儿,她已经可以和父母嬉戏了
Evelyn出生在2014年底,那时世界上根本没有特效药物用来治疗脊髓性肌萎缩症,这是父母的爱也无法改变的残酷事实。但在疯狂的网络搜索中,Evelyn的父母发现了一项正在招募受试者的临床试验,他们报了名。在Evelyn8个月大时,她接受了基因治疗。
而现在,原本被认为活不过两岁的Evelyn虽然不能像正常孩子一样跑跑跳跳,但却几乎完全健康地生活着,时常爬到妈妈的腿上嬉戏。而且不止是她,参与这项临床试验的全部15名患儿都活过了两岁!这不仅是属于Evelyn一家的奇迹,也是基因治疗在遗传病领域目前最为重大的突破之一!这项临床试验的结果登上了今天《新英格兰医学杂志》的头条。
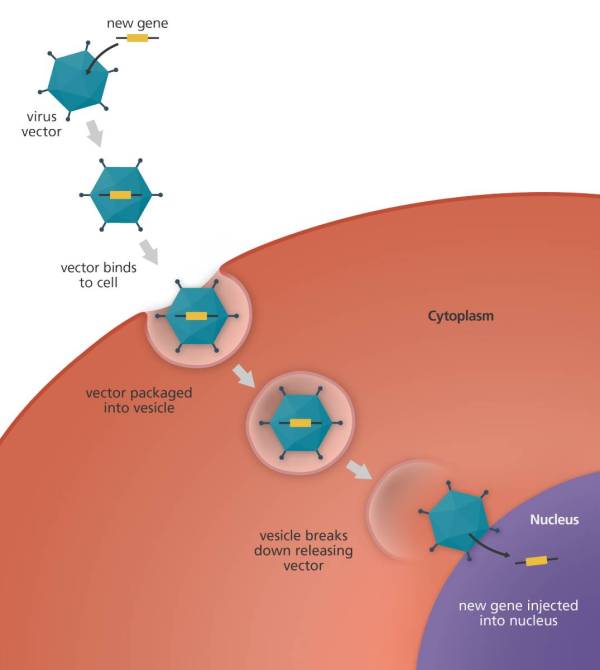 注射器一推,病毒给基因缺陷的细胞带来了及时雨
注射器一推,病毒给基因缺陷的细胞带来了及时雨
SMA此前被视为无药可医的遗传病,虽然发病率约为万分之一,但以中国每年出生1500万新生儿计算,这就相当于1500份直接发下的死刑判决书。“战争不是死去了数万人,而是死去了一个人这种事,发生了数万次。”对与病魔抗争的患儿和父母来说,这句话同样适用,而2016年的第一届中国SMA大会上发布的《中国SMA患者分析报告》指出,国内目前的SMA患儿预计有3-5万名。
SMA患者体内,一种名为SMN的蛋白质因编码基因SMN-1的功能缺失而异常,而SMN蛋白对运动神经元的存活至关重要。没了这种蛋白,神经元无法正常工作,就导致了肌无力,肌肉迟缓、萎缩,呼吸肌麻痹等多种症状的出现。针对这种机制,百健和Ionis制药联合开发的新药Spinraza于2016年12月获得FDA正式批准上市,SMA治疗专用药的空白才终于被填补。
Spinraza目前仍是SMA患者治疗的唯一专用药物
Spinraza的诞生中有着华人科学家的智慧,苏州大学教授华益民在开发中有着重要贡献,是相关专利的3位共同发明人之一。临床试验结果显示,这款新药通过对SMN-2基因的功能进行强化,增加SMN蛋白的数量,从而缓解疾病症状,使SMA患儿的死亡风险显著下降。但Spinraza仍然不能实现对SMA的根治,其高昂的价格(第一年花费为75万美元)也让很多患儿家庭望而却步。
在这个基因治疗的时代,既然SMA的发病与明确的基因缺陷有关,科学家们就决定从根本上解决问题。俄亥俄州立大学教授Brian Kasper的团队在利用腺相关病毒载体(AAV)进行基因治疗上进行了长期的探索,发现在腺相关病毒中,AAV9型可穿过戒备森严的血脑屏障进入大脑,将携带的SMN基因传递给神经系统细胞,从而在动物模型上实现了对SMA症状的治疗效果。
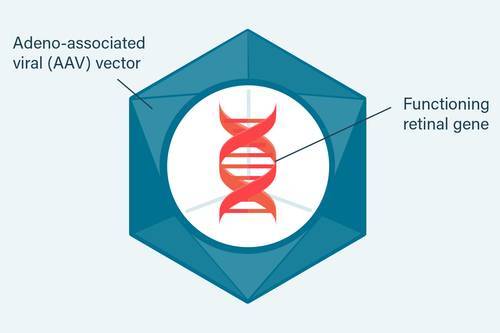 救命的基因乘上病毒载体的客船,去往远方
救命的基因乘上病毒载体的客船,去往远方
但是这种疗法却面对着一个巨大的问题:病毒毕竟不是智能机器人,被注射到血液之后,它们并不会定向行动,而会播散向全身各处,只有不到1%会进入大脑,因此如果想达到足够的治疗效果,注射的腺相关病毒量要达到此前基因疗法用量的100倍以上.
就算对病毒进行了灭活处理,它仍然还是一种病原体,治疗时会不会使患儿产生强烈的炎症反应?基于病毒载体的基因治疗在18年前就曾导致过悲剧,一名参加临床试验的18岁少年因为强烈免疫反应而死,这一领域曾经的明星科学家Jim Wilson也因此一夜沦为罪人。不过在悲剧后,Wilson教授没有放弃,他顽强地寻找着更加合适的病毒载体,最终他发现的120余种病毒载体有不少得到了业内认可,本次试验使用的AAV9最早就是出自他的实验室。
虽然灵长类动物试验体现了良好的安全性,FDA和相关部门也批准了试验,但2014年Kasper教授团队在全美儿童医院开始本次I期人体试验时,基因治疗界所有人的目光几乎都汇聚在此。悲剧会不会重演?
 首位死于基因治疗的少年Jesse Gelsinger(左)和当时试验的领导者,宾夕法尼亚大学Jim Wilson教授(右)
首位死于基因治疗的少年Jesse Gelsinger(左)和当时试验的领导者,宾夕法尼亚大学Jim Wilson教授(右)
第一位接受低剂量基因治疗的小女孩就把研究人员们吓出了一身冷汗,进行治疗注射后,她的谷丙转氨酶(ALT)和谷草转氨酶(AST)分别飙升到了正常水平的31倍和14倍,其他肝功能的指标也大多出现了明显异常,试验领导者,全美儿童医院的Jerry Mendell博士因此一夜都辗转反侧难以入眠。好在使用糖皮质激素抗炎处理后,小女孩的肝功能指标回落到了正常水平,此后两名出现类似表现的患儿也无大碍。
I期临床试验是药物或疗法步入临床的第一步,其目的往往是评估安全性和耐受程度,为后续试验确定合适的剂量,这也是本次试验最初的设计目标。但很快研究人员们就发现,接受基因治疗的孩子们肌肉无力、迟缓等症状明显改善,效果远远超出了预期。
用一组数据来说明基因治疗的杰出疗效吧:截至今年8月,接受治疗的所有15名患儿生存期都跨过了20个月大关,而此前的研究显示能活到20个月的SMA患儿只有8%;15名患儿中只有8名需要面罩辅助呼吸;接受高剂量(低剂量3倍)基因治疗的12名患儿中,11名都可独立坐起至少5秒钟,正常吞咽进食,而除了Evelyn之外,还有一名小男孩Matteo也实现了独立走路,Matteo甚至能短暂跑动。这对于SMA患儿来说是难以想象的,此前由于缺乏特效疗法,他们大多只能终日躺下,靠呼吸机等手段维持生命。Mendell博士表示:“我从来没见过基因治疗能在一种致命疾病上取得如此好的效果。”
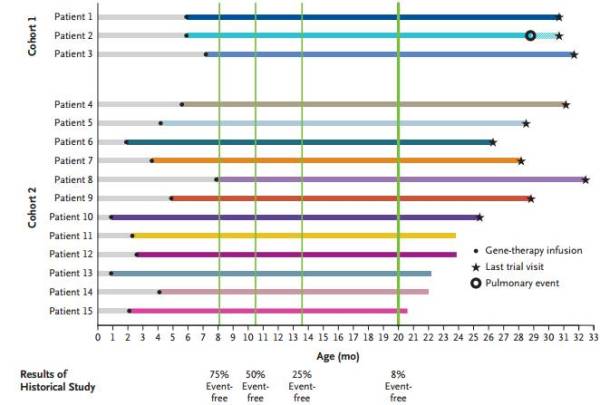 15名患儿生存期与SMA患者整体生存率的对照,基因治疗效果明显更好
15名患儿生存期与SMA患者整体生存率的对照,基因治疗效果明显更好
相较于已获批的Spinraza,腺相关病毒载体基因治疗的另一项巨大优势,则是理想状态下只需一次注射就可实现治疗,而Spinraza则需在维持治疗阶段每4个月进行再次注射。本次试验的结果也显示,基因治疗的安全性相当良好,患儿出现的不良事件基本仅限于转氨酶水平升高和呼吸系统疾病,并无危及生命的危险状况。
当然,也有科学家对基因治疗的长期效果表示了怀疑,毕竟本次试验的随访时间到目前为止也只有两年多,还无法对基因治疗的长期效果提前下断言。但获得该疗法开发权的生物制药公司AveXis已经开始了另一项针对SMA的临床试验,若试验成功,这种已被命名为AVXS-101,在去年获得FDA突破性疗法资格认定的基因疗法就将踏上步入临床的快车道。
而且,科学家们已经在探索更加高效的基因治疗载体。加州理工学院研究人员2016年在《自然-生物技术》上发表的研究成果显示,一种被称为AAV-PHP.B的新型腺相关病毒在进入中枢神经系统传递基因方面的效率是现有AAV9的40倍。有了这么强大的作用平台,基因治疗就能进一步大显神威了。
这也许真的是属于基因治疗的时代
如果进一步的研究和试验证明了该疗法的长期可行性和普适性,基因治疗将开启一个全新的时代,因为已有众多的遗传病被明确了大脑内的相关基因,而AAV9载体则是首个在临床试验中对中枢神经系统投递基因效果如此之好的载体,使用极大的病毒量取得治疗成功也是史无前例的。而且,由于AVXS-101基因疗法的靶点是神经元,因此补充的基因不会因为细胞分裂而作用逐渐减弱,应当可以维持多年的效力。
这对从事基因治疗的科学家们来说无疑是个好消息。由于副作用严重,此前获得欧盟批准用于脂蛋白酯酶缺乏遗传病的天价基因药物Glybera已于一周前退市,但本次的试验成果无疑是一针强心剂,北卡罗来纳大学的基因研究专家Steven Gray就表示:“人们将来回顾这次试验时,会把它看做一个里程碑,这标志着基因治疗将可以用于众多疾病。”
开发了首个SMA药物Spinraza的华益民教授说:“基因治疗效果确实很好,但是也存在一些风险。首先,有些患者会有一定的副作用;另外,虽然AAV病毒整合到基因组能力极低,但也有一定比例,存在致病风险。Sprinraza和基因治疗将是未来治疗SMA的两种主要方法。这次试验不是稍有提高,而是变革性的改变。这就是我们一直希望的基因治疗的样子。”
参考资料:
1.Lunn M R, Wang C H. Spinal muscular atrophy[J]. The Lancet, 2008, 371(9630): 2120-2133.
2.Finkel R S, McDermott M P, Kaufmann P, et al. Observational study of spinal muscular atrophy type I and implications for clinical trials[J]. Neurology, 2014, 83(9): 810-817.
3.http://www.sciencemag.org/news/2017/11/gene-therapy-s-new-hope-neuron-targeting-virus-saving-infant-lives
4.http://www.nejm.org/doi/full/10.1056/NEJMoa1706198
5.http://www.suda.edu.cn/suda_news/jxky/201612/85eddd7d-eb93-4b0f-be45-494c8a4361a6.html
6.http://www.nejm.org/doi/full/10.1056/NEJMoa1702752
7.http://www.npr.org/sections/health-shots/2017/08/01/540100976/drug-puts-a-750-000-price-tag-on-life
8.Foust K D, Nurre E, Montgomery C L, et al. Intravascular AAV9 preferentially targets neonatal neurons and adult astrocytes[J]. Nature biotechnology, 2009, 27(1): 59-65.
9.Foust K D, Wang X, McGovern V L, et al. Rescue of the spinal muscular atrophy phenotype in a mouse model by early postnatal delivery of SMN[J]. Nature biotechnology, 2010, 28(3): 271-274.
10.Gray S J, Matagne V, Bachaboina L, et al. Preclinical differences of intravascular AAV9 delivery to neurons and glia: a comparative study of adult mice and nonhuman primates[J]. Molecular Therapy, 2011, 19(6): 1058-1069.
11.http://www.nationwidechildrens.org/news-room-articles/phase-1-study-shows-encouraging-data-for-gene-replacement-therapy-for-spinal-muscular-atrophy-type-1?contentid=165924
12. Deverman B E, Pravdo P L, Simpson B P, et al. Cre-dependent selection yields AAV variants for widespread gene transfer to the adult brain[J]. Nature biotechnology, 2016, 34(2): 204-209.


{replyUser1} 回复 {replyUser2}:{content}