国内首款CAR-T细胞产品获突破性治疗品种认定 研发投入超7亿元
8月17日,上海复星医药(集团)股份有限公司发布的《关于复星凯特生物科技有限公司产品纳入突破性治疗药物程序》公告显示,其投资公司复星凯特的阿基仑赛注射液(商品名:奕凯达)用于治疗接受过二线或以上系统治疗后复发或难治性惰性非霍奇金淋巴瘤(r/r iNHL),包含滤泡性淋巴瘤(FL)和边缘区淋巴瘤(MZL)已被纳入突破性治疗药物程序。

医谷查阅CDE官网显示,阿基仑赛注射液“突破性治疗”申请公示截止日期为2021年8月16日。

来源:CDE官网
6月22日,复星凯特宣布国家药品监督管理局已正式批准其靶向人CD19自体CAR-T细胞治疗产品阿基仑赛注射液的新药上市申请,该药品成为中国首个按药品进行研发注册并获批上市的CAR-T细胞治疗产品,用于治疗既往接受二线或以上系统性治疗后复发或难治性大B细胞淋巴瘤(r/r LBCL)成人患者,包括弥漫性大B细胞淋巴瘤(DLBCL)非特指型(NOS)、原发纵隔大B细胞淋巴瘤(PMBCL)、高级别B细胞淋巴瘤和滤泡性淋巴瘤转化的DLBCL1。
阿基仑赛注射液是复星凯特引进美国Kite全球首个获批治疗非霍奇金淋巴瘤的CAR-T产品Yescarta(Axi-Cel)进行技术转移并获授权在中国进行本地化生产的靶向人CD19自体CAR-T细胞治疗产品。Yescarta是全球第二款CAR-T细胞疗法产品,于2017年10月18日获得FDA批准上市,其海外定价为37.3万美元(折合人民币约240万元)。2018-2020年,Yescarta销售额分别为2.64亿美元、4.56亿美元、5.63亿美元,复合年增长率为46.03%。
目前,阿基仑赛注射液已正式上市,但官方并未对外公布具体价格。网传该药品的价格为120万元/袋(约68ml)。根据复星医药今日发布的公告,截至2021年7月,复星凯特现阶段针对该产品累计研发投入约为人民币70354万元(含专利及技术许可费用,未经审计)。复星凯特目前正积极推进进入国家医保的事宜。7月30日,国家医保局公示了《2021年国家医保药品目录调整通过初步形式审查的药品名单》,阿基仑赛注射液位列其中。
图片来源:国家医保局官网
根据国家药监局今年7月发布的《突破性治疗药物审评工作程序(试行)》,药审中心将对纳入突破性治疗药物程序的药物优先配置资源进行沟通交流,加强指导并促进药物研发、加速上市。
截止目前,全球已有五款CAR-T疗法获批上市,除了Yescarta,还包括诺华的Kymriah、吉利德的Tecartus、BMS的Liso-cel以及其与蓝鸟生物共同开发的Abecma,除了Abecma是靶向BCMA外,其他四款均为CD19 CAR-T细胞产品。根据统计,2020年,在售的三款CAR-T产品合计销售额超过10亿美元。
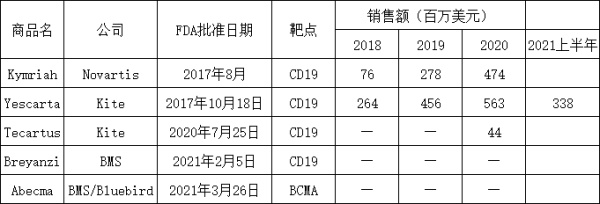
美国FDA已批准的5款CAR-T产品


{replyUser1} 回复 {replyUser2}:{content}