“胸怀大志”的靶点——Claudin18.2
Claudin18.2是当下最热门的靶点之一,就该靶点开发的创新药就包括单抗、双抗、CAR-T、ADC四种,几乎包含了当下最具前景和热门的生物创新药形式。即使是在已经被开发了多年的经典靶点当中,能够获此“殊荣”的也不多。
在国内,参与Claudin18.2布局企业有近30余家,四种路线全面覆盖。其中科济生物、石药集团、齐鲁制药、礼新医药至少都拥有2种(及以上)技术路线的靶向药。Claudin 18.2可谓是彻底的火起来了,其究竟拥有何种潜力如此被寄予厚望呢?
Claudin(CLDN)是人体正常组织中紧密连接最重要的一种蛋白质,具有4个跨膜结构域,是细胞紧密连接的重要分子,参与机体生理过程如细胞旁通透性和电导的调节,其构成了细胞旁屏障,控制着细胞间分子的流动。该家族包含至少27个成员,其中Claudin18有Claudin18.1和Claudin18.2两种异构体,而Claudin18.2主要应用于胃癌以及胰腺癌方向的适应症。
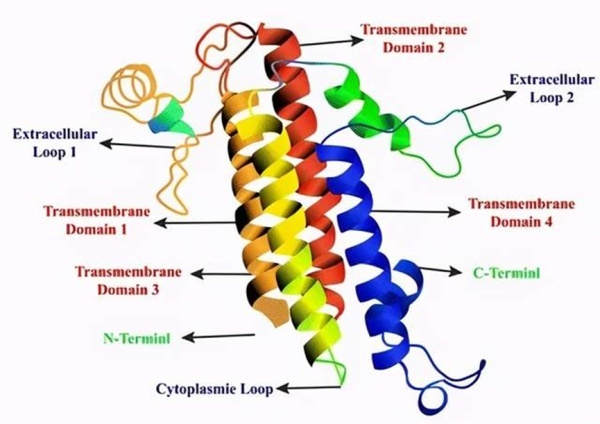
Claudins蛋白结构
胃癌患者人数在所有的恶性肿瘤中排名第四,造成的相关死亡率中排名第三,尤其是我国还是一个胃癌大国。但目前临床上与肺癌相比,胃癌获批的靶向药物非常少,获批的适应症仅仅“老牌“靶点HER2以及抗血管生成抑制剂VEGFR2,这代表了胃癌的靶点治疗存在大量需求。国内众多药企布局Claudin18.2,也是为了争夺目前还未"染红"的"蓝海"市场。
HER2靶点在胃癌患者中的阳性率仅仅10%-15%,而Claudin18.2在胃癌中呈现出高表达的特性,阳性率超过60%。对于胃癌患者来说,Claudin18.2是一个极为理想的打击靶点。
不仅如此Claudin18.2在除了胃癌之外的多种肿瘤组织中高度表达,如胰腺癌(50%)、食管癌(30%~50%)和肺癌(40%~60%)等,但是在正常组织中几乎没有表达,Claudin 18.2具备出色的特异性。
有一项研究发现,在已扩散到卵巢的胃癌患者中,69%的卵巢癌细胞存在明显的Claudin18.2蛋白。这意味着对于大部分已转移的晚期癌症患者而言,Claudin18.2靶向药同样有效。
Claudin18.2几乎为靶向药而生。不仅仅是其本身优异的靶向属性,还瞄准了胃癌以及胰腺癌目前治疗的空白空间,其市场价值不可估量。这种背景下,国内外药企纷纷进军Claudin18.2 靶点争相布局的原因或许并不让人意外。
在全球Claudin18.2靶点布局上,国内药企最为积极,竞争程度最为激烈。在除了单抗之外,国内药企布局的Claudin18.2靶点的ADC、双抗、CAR-T的进度目前全面领先,且占比80%以上。这也导致了海外药企纷纷引进国产Claudin18.2 药物,迎来密集出海期。
延伸阅读:PD-1之后,国内Claudin18.2靶向药凭何成为出海香饽饽?
以下将对全球范围内进展较快的Claudin18.2药物进行部分展开介绍:
单抗:安斯泰来的Zolbetuximab是第一个针对于Claudin18.2靶点的单抗药物,也是目前进展最快的靶向Claudin18.2抗体药。在2016年ASCO年会上由Ganymed公司第一次公布了IMAB362的临床数据:采用Zolbetuximab治疗,患者的无进展生存期和总生存期延长了近一半!
随即,Claudin18.2作为新兴靶点引起了业界的关注,安斯泰来以14亿美元的价格收购了Ganymed公司,并获得了Zolbetuximab的开发权力。
在去年公开的2期研究数据中也证实,Zolbetuximab治疗晚期胃癌或胃食管交界处癌或食道腺癌患者,临床获益率达到23%。同时,从分组分析中可以明显地看出,Zolbetuximab对于Claudin 18.2表达水平更高、尤其是表达水平≥70%的患者疗效更加显著。
目前Zolbetuximab有两项适应症在临床研究中,用于治疗胃或胃食管连接处腺癌的3期临床和用于治疗胰腺癌的2期临床,有望成为全球首款上市的Claudin18.02单抗。
在国内科济药业的AB011是我国自主研发的首个针对Claudin18.2的单抗,目前,AB011正在我国开展治疗Claudin18.2阳性实体瘤的I期临床研究;进度最快的是创胜集团的TST001,产品已经进入临床2期,全球进度上仅次于安斯泰来的Zolbetuximab。
ADC:康诺亚生物的CMG901,是全球首个Claudin 18.2 ADC药物,由康诺亚与乐普生物旗下美雅珂联合研发,2022年4月,康诺亚宣布CMG901用于治疗复发/难治性胃癌及胃食管结合部腺癌已获美国FDA孤儿药资格认定和快速通道资格(FTD)。
双抗:2021年3月4日,启愈生物的Q-1802成为国内首个申报临床的Claudin18.2/PD-L1双特异性抗体;安进/百济神州的AMG 910为半衰期延长 (HLE) 抗 CLDN18.2 x 抗 CD3 双特异性T细胞接合剂 (BiTE) 分子,是首个进入临床阶段的Claudin 18.2双抗,目前正在全球处于胃癌或胃食管交界处癌的I期临床阶段。
CAR-T:2022年3月3日,科济药业公司自主研发的CAR-T细胞候选产品CT041获中国国家药品监督管理局(NMPA)药品审评中心(CDE)同意进入确证性Ⅱ期临床试验,主要治疗既往接受过至少二线治疗失败的Claudin18.2(Claudin18.2)表达阳性的晚期胃癌/食管胃结合部腺癌(GC/GEJ);传奇生物开发的靶向Claudin18.2的CAR-T细胞疗法LB1904已经进入临床I期试验,用于治疗胃癌或胰腺癌。另外,传奇生物还启动了一项评价三个靶向Claudin 18.2的CAR-T细胞制剂LCAR-C182A /LCAR-C182B /LCAR-C182C治疗晚期胃癌和胰腺导管细胞癌安全性、耐受性和有效性的开放性I期临床研究。
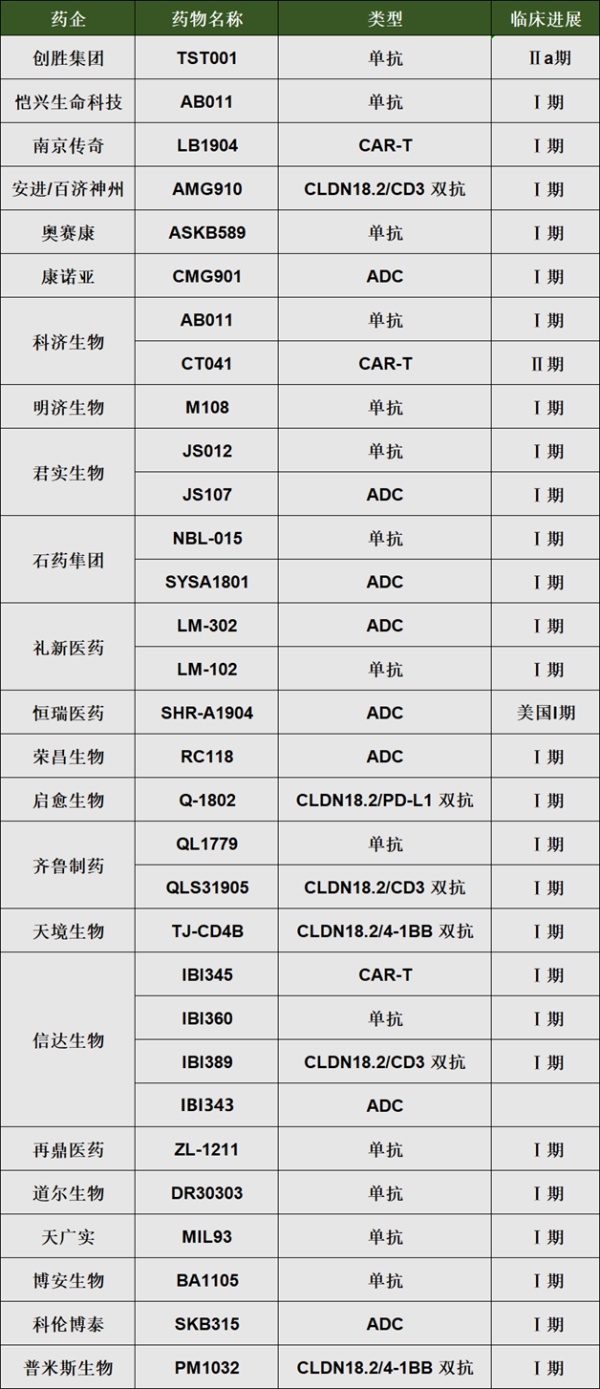
国内部分Claudin18.2布局进度
Claudin18.2是一个极具潜力和价值的靶点,是目前癌症靶向治疗空白领域的理想补充。虽然现阶段未有药物上市,但国内众多企业均已布局不同疗法,争取在这市场中占据一席之地。在国际赛场上能够吸引海外药企的目光,也足以证明国内药企的研发实力。期待早日看到国内的Claudin18.2靶向创新药成功上市,造福更多的患者。
来源:dessert 佰傲谷BioValley


{replyUser1} 回复 {replyUser2}:{content}