基因治疗已经迈入快速增长的黄金时代,AAV基因疗法自从2017年FDA批准罗氏/Spark的Luxturna上市以来,逐渐已经成为目前最热门的细分赛道之一。目前,从商业化的角度来看,基因治疗产品行业可以分为上游病毒载体生产产商(包括试剂耗材及设备)、中间制药企业,下游各类罕见病/遗传病患者三大块。
近几年来基因治疗赛道持续火热,各大药企积极布局AAV基因疗法,那么已上市的AAV基因疗法在全球的销售情况如何呢?其商业化之路能给我们带来哪些启示?Glybera通常被视作全世界“首个”基因治疗药物。2012年,Glybera获得EMA批准,成为西方市场首个批准上市的基因疗法,成为基因疗法商业化的里程碑事件。该产品借助腺相关病毒(AAV)载体将产生功能性脂蛋白脂肪酶的基因递送到患者骨骼肌,用以治疗脂蛋白酯酶缺乏症,达到降低胰腺炎发病率的效果。然而,直到2017年宣布退市,也仅有一名患者接受过Glybera治疗。虽然是彼时最昂贵的药物,但即便以标价计算,Glybera销售额也只有100万美元。➤ Luxturna
Luxturna于2017年底获得FDA批准,治疗RPE65突变相关的视网膜营养性萎缩,成为首款矫正基因缺陷的基因疗法。2018年,Luxturna®又顺利获得EMA批准。该疗法以腺相关病毒(AVV)为载体,搭载并向患者体内导入健康的RPE65基因,使得RPE65基因可以发挥正常作用,治疗眼疾。
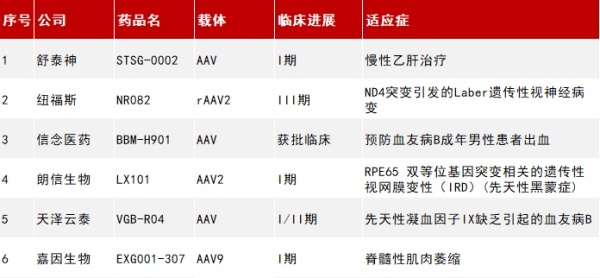
根据Spark财报显示,上市以来Luxturna共取得5500万美元净销售额(2018-2019年9月:2700万美元和2800万美元)。2019年10月罗氏宣布收购Spark,此后Luxturna的销售情况未能继续体现在罗氏财报中。据业内人士表示,其在美国未来十年获利可能仅为每年6000万美元,目前还没有在中国销售的计划。Zolgensma于2019年5月获得FDA批准上市,适用于治疗2岁以下脊髓性肌肉萎缩(SMA)、生存运动神经元1(SMN1)基因双等位基因突变的儿童患者,定价212.5万美元。Zolgensma的知识产权拥有者原为AveXis,2018年4月,制药巨头诺华宣布,以87亿美元现金大手笔收购美国基因治疗公司AveXis,一举将Zolgensma纳入麾下。据诺华的财报,2020年Zolgensma的销售额达9.2亿美元,同比增长151%;2021年迈入“10亿美元俱乐部”,销售额为13.51亿美元,同比增长46%;2022上半年销售收入7.42亿美元,同比增长22%,可谓是目前已上市AAV疗法中商业化最为成功的一个。目前Zolgensma®已经在国内启动临床,此外在新兴市场方面,中国成为诺华最关注的地区之一,诺华的明星产品早已在国内布局。据诺华制药全球总裁Marie-France Tschudin称,诺华肿瘤和诺华制药2021年预计在中国还会有7个新产品获批,中国区将成为诺华极具潜力的新兴市场。2022年7月20日,欧盟批准Upstaza,用于治疗年龄在18个月及以上、临床、分子和遗传学确诊为AADC缺乏症并伴有严重表型的患者,其定价暂未披露。回顾已上市的4款AAV销售额,其中Zolgensma®销售量最佳,成为唯一一款“重磅炸弹”。但高昂的售价是基因治疗时常被诟病的一个槽点,如Zolgensma在2019年获批上市后立刻被美国各大媒体冠以“史上最贵疗法”。面临高昂价格的争议,基因治疗药企也在积极与各国保险进行积极探索,开发出了各种基于价值的支付模式。如Anthem等公司采取分期付款的方式覆盖了Spinraza、Zolgensma等药物,这些有益尝试在保证了患者受益的同时,也为基因治疗药物的商业化逐步铺平道路。例如诺华鼓励保险公司承保Zolgensma ,允许患者在5年内以每年42.5万美元进行分期支付,这一措施缓解了患者支付压力,同时也推动了Zolgensma的销售增长。药物的专利保护也是定价高的一项重要原因,一个药物的成功研发到生产至少需要10年,并且投资巨大。为防止仿制药对专利药的恶意竞争,新药研发非常需要专利的保护。在专利保护期内,制药公司可以任性定价,并受政府获许的垄断性保护,其他公司不得开发,更不能出售类似药物。这也是制药公司不断研发新药的主要动力。所谓任性定价并不是漫天要价,一些药物药价评测机构会基于循证医学等各种建模与评测方法,根据药物研发和生产的成本,医院和患者使用的效果,以及综合政府保险承受力等多方因素,给药物评估一个合理的价格。在这样严密的制衡下,药品的定价也就不能突破市场的承受极限。考虑到基因治疗方式的特殊性,理论上一次给药,长期有效,即“一劳永逸”的疗效,最终的治疗费用较目前多数疾病的传统长期疗法实则更低,另外,还减轻了患者多次长期治疗的痛苦。正如Zolgensma和Spinraza同为SMA的基因治疗药物,虽然Zolgensma的价格是Spinraza的十倍,但Zolgensma只需要一次治疗,而Spinraza则需要每年一次。患者似乎对前者的治疗周期与方式更为青睐。以一位血友病患者的传统治疗为例,一年的治疗费约30万美元,那么一生的长期治疗费用约500万~1000万美元,由此看出,基因治疗较高的定价有一定的合理性。但高价基因治疗临床应用也会受阻于当前的支付制度。所以,要想使基因治疗全面市场化,必须挑战现行支付制度。根据行业内大多数观点,潜在的支付方式主要有以下3种:(1)一次性付费模式,这是药企最期望的支付方式,但是对于患者来说费用过高。(2)分期付款模式,类似目前的贷款消费,分期还贷。(3)按疗效付费模式,对于患者也许是最合理的支付模式。“按疗效付费”是基于疗效和医疗服务绩效的付费管理模式,其核心就在于维护与促进病人健康。通过协议、合约形式,实行医保单独付费管理,有利于推动和促进医疗新技术、新项目与创新药的研发与推广。考虑到基因治疗“一劳永逸”的特效,据治疗后每年的确切疗效为当初的治疗分期付费,既分摊了治疗费用,减轻了患者当前的支付负担,也让患者在确切治疗效果面前愿意付费,但让药企担心的是如何有效保障支付者按期合理付款。无论如何,只有患者与药企能够实现双盈,才能推动AAV基因疗法持续稳健发展。虽然国内尚未有AAV基因治疗上市,但国内自研AAV基因疗法已经离上市不远,其定价与商业化也必然值得关注。目前国内已有8家企业的基因治疗产品获批临床,其中纽福斯生物在眼科基因治疗临床上最为领先,其首款候选药物NR082眼用注射液于2021年3月获得国家药品监督管理局(NMPA)药物注册临床试验(IND)许可,是国内首个获得临床试验许可的眼科体内基因治疗药物,拟用于ND4突变引起Leber遗传性视神经病变(LHON),目前即将进入临床III期。▲ 国内已获批临床的在体基因疗法(星耀研究院整理)那么,根据国外已上市的几款AAV基因疗法商业化经验,有哪些方面是值得我们借鉴与注意的呢?根据弗若斯特沙利文的数据显示,2025年我国基因治疗市场规模将达到179亿元左;假设在2025-2027年之间,我国基因治疗CAGR增速与全球保持一致,我国基因治疗市场规模将达到500亿元左右。从市场角度,应该吸取Glybera®撤市的教训,过小的市场需求和过高的定价会导致产品即使上市也可能半路夭折。但是中国作为人口大国,即使是罕见病,也仍然有较可观的市场需求。而且,国内对罕见病开发也是大力支持和倡导的,并出台相关政策保障药企利润空间,如审批流程简化、分类实施快速审评、长达7年的市场独占期等。昂贵的药物只能在与卫生部进行艰难的价格谈判后才能报销。这通常涉及治疗罕见疾病的药物,即所谓的"孤儿药"。谈判已成为昂贵孤儿药市场准入过程中的一个重要组成部分,在这一过程中,研发费用要与患者的痛苦相权衡,这对各方来说都是一项艰巨且具有道德争议的任务。不纳入医保,患者就无法得到治疗,药厂就不能生存。而2021年国家医保药品目录谈判中,7种罕见病用药纳入医保目录,其中包括备受关注的用于治疗脊髓性肌萎缩症(SMA)的Spinraza。2022年1月1日,Spinraza单针价格从70万元降至3万多元。今年,全国多地已有多名患儿用上了Spinraza。这种“天价药物”进入中国市场后,为何能如此大幅降价,业内人士表示,降价达成的个案突破,这也是药企战略选择中的一种策略。近年来,国内的一系列政策大大降低了罕见病创新药进入中国市场的成本,在注册准入和医保准入上,都为创新药企业提供了更好的政策环境。由于加速审评审批的政策利好及患者基数高,在中国开展的基因治疗临床数量已达到全球第二,未来中国对基因治疗产品临床试验和后续商业化吸引力将持续提升。国内已批准上市的罕见病用药中,超过 2/3 的比例被纳入国家医保,以及更大比例的产品被纳入部分省市的地方医保。此外,罕见病药物进入临床后获得批准的概率较高,审批时间会短一些,也就意味着更高的投资回报率。虽然罕见病患者人群基数小,但该领域有着未满足的重大需求。科创板上市标准的第五条—“市值+技术优势”,对纽福斯这类尚未有营业额的企业敞开了上市通路,上市后企业有了名气,其产品也会进入患者的视野,并获得盈利。而2021年的医保目录谈判,则实现了高值罕见病药物在国家医保目录中的“零突破”,期待未来有越来越多的AAV基因治疗进入国内医保,让患者更有“医靠”。与其他药物相比,基因疗法非常昂贵。开发人员在药物基础研究,工艺研发和生产方面进行了大量的前期投资,这些投资最终细化到了患者身上。专门从事检测分析的实验室旨在标准化及简化流程,以降低基因治疗药物生产成本,从而减轻患者及其家属的经济负担。一款新药的销售额还取决于各家药企的销售能力,而国内大多数AAV企业都是Biotech,相比较于销售能力成熟的Biopharma而言,这方面能力可能略显不足。在未来,选择与大药企合作销售,还是寻求与政府或医院合作,自建销售渠道,都不失为一种销售策略。至于药品定价,更多可能需要从降低AAV生产成本入手,同时增加疾病人群的覆盖面(从罕见病到常见病),以更合适的价格更优质的疗效推向患者群体,才能在医药市场竞争中赢得一席之地,这也是所有医药企业与CDMO共同努力的方向。来源:Luc 星耀研究院


{replyUser1} 回复 {replyUser2}:{content}