减肥也能轻松“躺赢”?在研减肥疗法分析窥见三大积极趋势
在2022年这个史上最热夏天,燃烧卡路里又成为大多数人的迫切需求。关于如何减肥,健身、节食是刻进人类DNA里的方法,而药物总给人留下不安全、没效果的印象。然而近期,一些减肥疗法取得了相当积极的进展:《自然》子刊的一篇论文找到了降低腹部脂肪的关键基因突变,未来可能只需要一年打一针便能消除“游泳圈”;礼来在《新英格兰医学杂志》上公布了糖尿病治疗药物tirzepatide的3期临床试验结果,72周的治疗周期后患者减重最高可达22.5%,树立了减肥药减重效果新标杆。
药物开发趋势一:靶点多元化
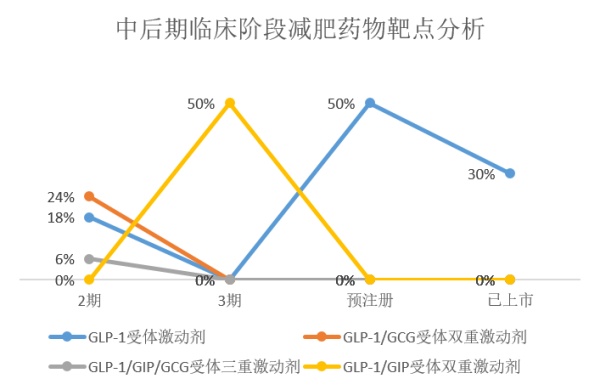
以GLP-1受体激动剂为代表的肠促胰岛素(incretin)疗法在各个阶段疗法中均占主导地位。 处于2期临床开发阶段的疗法靶点种类更加丰富,机制更为新颖,包括可控代谢加速器、神经肽YY5受体,IKKε/TBK1,激活素Ⅱ型受体等,3期及更高状态疗法靶点相对较为单一。
药物开发趋势二:未来将大力发展口服剂型
药物开发趋势三:减重效果突破瓶颈
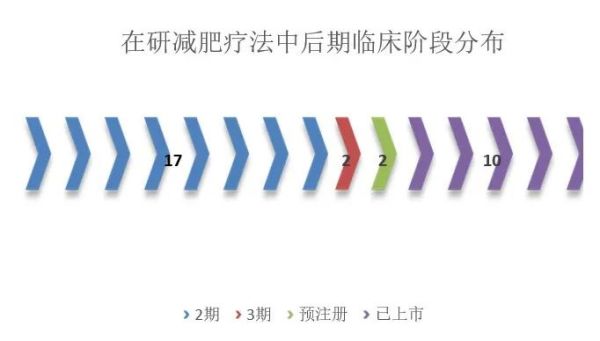
靶点:GLP-1受体主导,多重机制肠促胰岛素高速增长
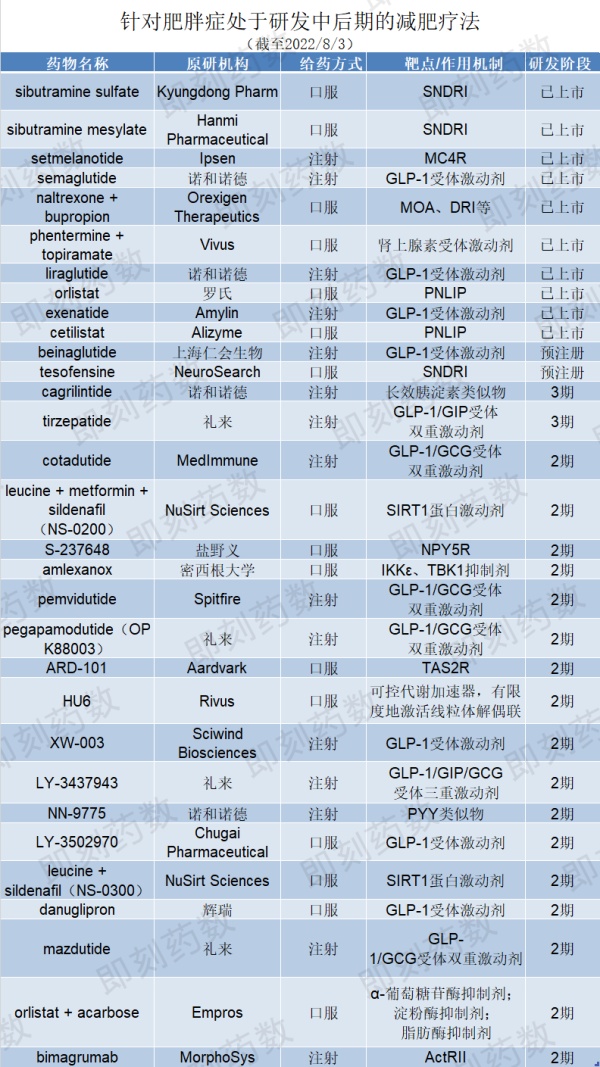
除肠促胰岛素这一类靶点外,从已上市到2期阶段,疗法总体呈现出靶点愈加多样化、新颖化的趋势。已上市的10款药物中有5种针对非肠促胰岛素靶点,sibutramine sulfate和sibutramine mesylate属于5-羟色胺-去甲肾上腺素-多巴胺再摄取抑制剂(SNDRIs),orlistat和cetilistat靶向胃肠道脂肪酶,naltrexone + bupropion分别靶向阿片受体与肾上腺素能受体,这些靶点的历史较为悠久。
预注册的2款疗法中除了GLP-1受体激动剂外,tesofensine依然是SNDRIs。而到了3期疗法中,tirzepatide是GLP-1/GIP受体双重激动剂,cagrilintide是长效胰淀素类似物。胰淀素(amylin)是一种与胰岛素共同分泌的多肽,它通过调节饱腹感的信号通路降低食物摄入。
最后在17款进行2期临床试验的疗法中,非肠促胰岛素作用机制共有8种,分别为可控代谢加速器(CMAs)、神经肽YY5受体、食欲调节激素、代谢疾病的重要调节因子IKKε/TBK1、SIRT1蛋白、激活素Ⅱ型受体、苦味受体TAS2R、淀粉酶/葡萄糖苷酶,这些机制相对而言较为新颖。苦味受体不但在口腔中介导苦味的感知,而且在身体的其它组织中也有表达。Aardvark Therapeutics的ARD-101与肠道细胞表面TAS2R的结合可增加GLP-1等内源性肠肽激素的表达,从而产生全身性代谢调节作用。HU6是一种可控代谢加速器(CMAs),可有限度地激活线粒体解偶联,通过将质子从线粒体膜间隙中运出,能促进糖和脂肪氧化的增加,同时维持三磷酸腺苷的产生水平不变。激活这一过程会导致脂肪积累减少,并防止全身额外的脂肪积累。早期临床疗法中新型靶点的不断涌现反映出产业正积极探索治疗减肥的创新策略。
剂型:口服略多于注射,未来口服剂型发展趋势更佳
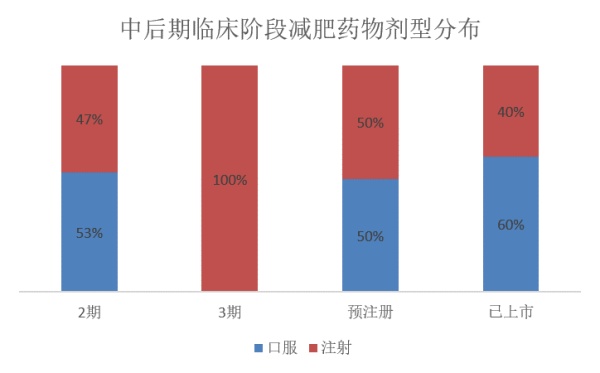
在31款药物中,口服药物有16款,注射药物有15款。按照临床阶段细分,已上市药物中口服形式占比60%,而在预注册和2期临床阶段,口服药物比重下降为50%和53%,正在进行3期临床试验的2款药物都通过注射给药。在已上市和预注册状态的药物中,以GLP-1受体激动剂为代表的肠促胰岛素疗法的给药途径均为注射,只有在2期临床阶段,7款肠促胰岛素疗法中才出现2款通过口服给药。从中可以看出肠促胰岛素疗法由于半衰期较短,采取注射比口服能达到更佳的药物吸收效果。这也解释了口服疗法比重在不同临床试验阶段下的波动,在已上市、预注册、3期状态下,由于肠促胰岛素疗法比重的攀升口服药物比例随之下降,在2期阶段,随着靶点的多元化分布和口服肠促胰岛素疗法的开发,口服药物所占百分比再度回升。放眼未来,口服减肥疗法的发展趋势或将优于注射,因为口服的用药依从性显著高于注射,从肠促胰岛素这样本身难以制成口服剂型的药物正被探索用于口服可以推测产业将投入更多资源开发减肥药物的口服制剂。
减重效果:“后来者”居上,上限不断提升
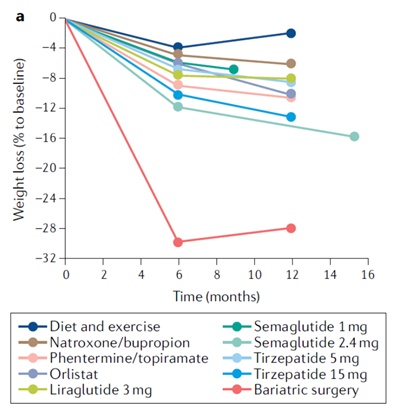
▲不同减肥疗法降低体重的效果(图片来源:参考资料[1])
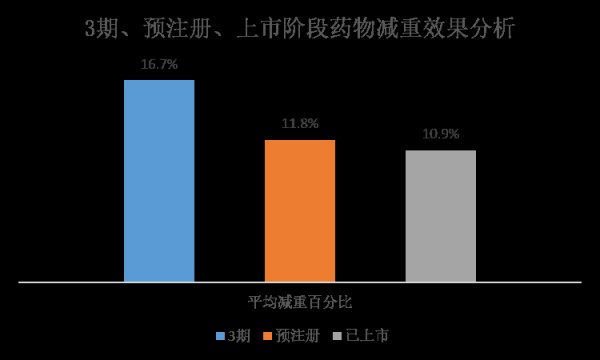
来源:药明康德
版权及免责声明:本网站所有文章除标明原创外,均来自网络。登载本文的目的为传播行业信息,内容仅供参考,如有侵权请联系答魔删除。文章版权归原作者及原出处所有。本网拥有对此声明的最终解释权。


{replyUser1} 回复 {replyUser2}:{content}