国外mRNA已吸金百亿美元,国内千亿蓝海何时引爆?
从“无人问津”到“门庭若市”,历经数年,mRNA技术因新冠疫苗之故迅猛发展。2020年两款mRNA疫苗的上市正式宣告mRNA技术进入商业化时代,mRNA技术变得炙手可热,已成为一项跨时代的生物技术。除了广为人知的新冠疫苗,国外巨头也早已在其他疾病领域布局。
近日,Moderna公司也召开了一年一度的研发日活动(R&D Day)。在研发日活动上,Moderna表示,基于mRNA技术在疫苗领域的概念验证,该公司目前已经有24款疫苗进入临床开发阶段,是3年前的3倍。其中4款疫苗处于3期临床开发阶段。此外,该公司也在进行mRNA技术作为酶替代疗法的概念验证,初步临床试验结果显示可喜的安全性和疗效。
但回看国内,当国外药企在担忧新冠疫苗市场饱和之时,在中国mRNA领域打头阵的新冠疫苗却还未能获批。因此,国内有很多人对此赛道产生了一定的疑虑和担心,到底国内mRNA什么时候能真正地迎来辉光?
商业化方面
2021年辉瑞/BioNtech新冠mRNA疫苗销售额为404亿美元,荣登2021年全球畅销药TOP1,销售额接近第二名的2倍;同时,Moderna的mRNA疫苗Spikevax(mRNA-1273),2021年全年卖了8亿多剂,营收177亿美元。今年上半年,更是实现营收108亿美元,同比增长了71%。
国外两款上市的mRNA新冠疫苗,均取得了巨大的商业成功,收到大量来自各国政府及机构的巨额订单,跻身2021年全球畅销药的TOP5。特别是Comirnaty,位居畅销药榜首,展现了极大的商业化价值,Moderna公司更是凭借Spikevax从一个名不见经传的企业摇身一变成为当红“炸子鸡”。
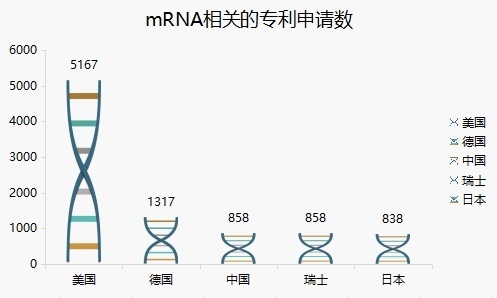 ▲ mRNA相关的专利申请数(图片来源:根据Astamuse数据整理)
▲ mRNA相关的专利申请数(图片来源:根据Astamuse数据整理)
日本经济新闻社出资的数据分析企业Astamuse分析了2001年至2022年2月的mRNA相关技术的专利申请情况。在全球申请的10864项专利中,按国别来看,首位是美国,高达5167项,占整体的48%。其次是德国(1317项)、中国(858项)和瑞士(同前)。日本以838项排在第5位。
成为研发核心的是美国和德国,按具体申请方观察专利数量,德国CureVac以745项排在首位。美国Moderna(272项)和德国BioNTech(79项)等涉足新冠病毒疫苗的企业也跻身前列。全球范围来看,专利数量走在前面的几乎清一色是国外的企业。据相关数据分析,TOP10的公司拥有全球mRNA产品80%以上的专利申请数量。
虽然mRNA赛道在国外已进展得如火如荼,但是mRNA毕竟是被疫情“催熟”的技术,其安全性等方面还需多加观察。譬如欧洲药品管理局(EMA)曾报道,有小部分人在接种完辉瑞和Moderna的新冠疫苗后产生了三种新症状,包括多形红斑(Erythema multiforme)、肾小球肾炎(glomerulonephritis)/肾脏炎症、肾病症候群(Nephrotic syndrome)。另外,美国疾病控制与预防中心(CDC)也发现,青少年群体中罕见的心脏炎症,可能与使用了mRNA技术的新冠疫苗接种存在关联。除此之外,新冠疫苗因其一定的特殊性,对于mRNA药物的长期有效性与重复使用安全性,还待进一步验证。
因此,此次吃到疫情红利的国外企业,可以说是尝到了mRNA市场的第一块甜点,大餐还在后面。作为一项新兴技术,mRNA技术还需要依靠时间的沉淀才能逐步完善,而这恰好能成为国内企业“弯道超车”的一个机会。
企业管线进展
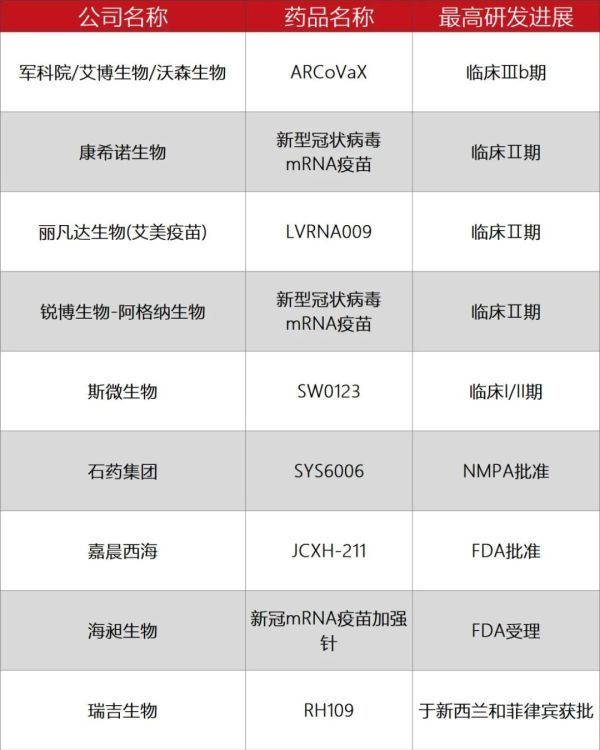
➤ 今年4月,康希诺生物和石药集团先后宣布了其研发的mRNA疫苗获得了NMPA批准,开展临床试验。其中基于在安全性、有效性以及产业化方面的优势,并根据疫情防控的需要,石药集团的新冠mRNA疫苗SYS6006还被NMPA列入特别审批程序,快速批准进入临床。
➤ 2022年6月27日,瑞吉生物宣布,其研发的冻干新型冠状病毒Omicron株mRNA疫苗RH109由下设合资公司分别在新西兰和菲律宾获得临床批件。本次获批,标志着全球首款冻干型新冠Omicron株mRNA疫苗进入临床阶段,具有里程碑意义。
➤ 2022年8月16日,嘉晨西海的自复制mRNA肿瘤疫苗JCXH-211注射液临床试验获受理,这是国内首款申报临床的基于自复制mRNA的编码人白细胞介素-12(hIL-12)的新型药物。嘉晨西海绕开新冠疫苗,在mRNA的应用上率先朝疾病治疗迈出了一步。
截至目前,除了从辉瑞/BioNTech引入复必泰的复星医药之外,军科院/艾博生物/沃森生物的ARCoVaX仍是临床进展最快的,已进入Ⅲb期,有望成为国内首款上市的mRNA疫苗。一旦成功获批,也就意味着这当中的技术与监管环节在国内被打通,后续将迎来一波发展热潮。
来自中商产业研究院的数据,中国mRNA领域投融资金额在2016-2019年一直在1亿美元每年的范围,从2020年开始大幅增加至7.66亿美元,刚过去的2021年达到新高,为13.61亿美元。
而实际上,新冠疫情之后,作为新冠疫情的防控利器,新冠疫苗透支了整个疫苗行业近三年的关注和投资市场景气度,国内现在的mRNA疫苗市场已经稍微冷淡。从2021年高点算下来到如今的2022年,mRNA疫苗的两个领头企业,沃森股价腰斩了53%,复星最低跌了56%,而mRNA新冠疫苗国内如今还未获批。
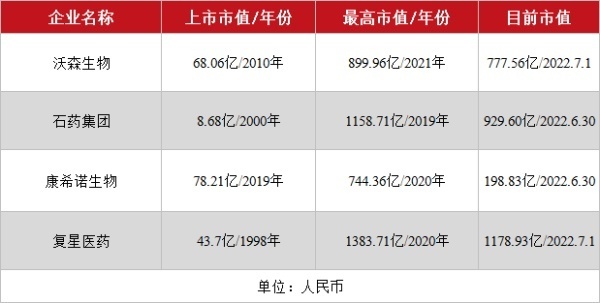
▲ 国内mRNA疫苗上市企业的市值变化(图片来源:星耀研究院整理)
由上表可以看出,国内在做mRNA疫苗的企业,近来并未获得资本的青睐,估值大多都在2020-2021这段时间达到巅峰值,然后一路下跌,特别是只专注于布局mRNA疫苗而没有其他候选管线的企业。
即便如此,mRNA赛道上的企业并没有因为资本的稍微缓和而冷落管线的研发,而是仍然在孜孜不倦地探索mRNA创新技术,努力突破国外技术和专利壁垒,开拓出一条属于国人自己的mRNA康庄大道。因此,随着国内mRNA技术的不断成熟,资本依然看好那些具有创新突破性技术与应用领域的企业。
在mRNA新冠疫苗之前,全球都尚未有一款mRNA疗法获批。而2020年初疫情爆发,随着两款mRNA新冠疫苗的上市,引发了广大民众对mRNA疫苗的热情和期待,全球资本大量涌入mRNA领域。虽然国内资本市场同样也竞相角逐此赛道,并在2021年到达高点,但此后mRNA便坐上了“冷板凳”到现在。究其原因,是国内的mRNA领域相比国外来说还有一些差距,但值得欣慰的是,国内相关企业并未坐以待毙,而是努力地寻求突破口。
截至2022年9月,当国外药企都担忧新冠疫苗市场饱和时,中国的mRNA新冠疫苗却还未能获批。根本原因是这批2019年前后才刚成立的中国mRNA疫苗企业,技术储备远不如十多年前就成立的Moderna和BioNTech。
除了相关技术需要验证,还有另一个因素也值得注意:在mRNA的各个环节中,亦处处埋伏着欧美企业所设置的专利壁垒。
不过国内也在序列设计和递送系统等平台技术方面做出了很多自己的创新。包括:百度研究院推出全球首个mRNA疫苗基因序列设计算法LinearDesign、基因编辑先锋人物张锋及团队开发了SEND递送技术……这些都为国内的mRNA发展注入了巨大的新能量。
➤ 2020年8月,NMPA药品审评中心曾颁布《新型冠状病毒预防用mRNA疫苗药学研究技术指导原则(试行)》,主要针对非自我扩增型mRNA疫苗,明确现阶段对mRNA疫苗药学研发技术的基本要求。
➤ 2021年10月,WHO通过文件Evaluation of the quality, safety and efficacy of messenger RNA vaccines for the prevention of infectious diseases: regulatory considerations,WHO文件提供了关于人用预防性mRNA疫苗的生产和质量控制,以及非临床和临床评估的关键方面的信息和监管考虑。
➤ 今年2月,美药典USP出具了《mRNA疫苗质量分析流程》草案,支持mRNA疫苗和疗法的质量评估,帮助公司和监管机构更快地将创新药物推向市场,USP希望通过质量共识加速产品开发。此外,美国FDA还对mRNA疫苗的上市之路一路开绿灯,包括加速mRNA疫苗的上市审评、甚至拜登政府直接动用《国防生产法》(Defense Production Act,DPA),让辉瑞快速采购到过滤乙醇的设备。
而此前,国内还尚未有一项完整的、具体的针对mRNA审批的法规、政策,大部分国内企业仍需参考一些其他品种或者国外出台的政策法规。这样,国内的mRNA产品就很难有一个统一的、可供参考的标准,因此质量也难免参差不齐,同时也加大了临床审评的困难,放慢了临床审评的速度。
不过为指导我国新冠疫苗的临床研发,提供可参考的技术标准,在国家药品监督管理局的部署下,国家药监局药审中心发布了《新型冠状病毒预防用疫苗研发技术指导原则(试行)》等5个指导原则的通告。以及我国的“十四五”医药工业发展规划也提倡大力发展mRNA技术。因此随着我国法规的不断完善,我国的mRNA企业也能够更快地脱颖而出。
这一点不是我国专有,作为一项新兴技术,mRNA领域无论在国内还是国外,人才缺乏现状都较为严重。而人才缺乏的问题并非短时间内就能解决,而是需要积累。在核酸药物这个领域,人才都相对年轻,但国内整体态势是比较好的,企业积极性很高。同时,国内也在大力引进国外的专家和高级人才,国内的产学研也协同培养创新型的医药人才。
国内也具有一些潜在的优势:一方面是有大量的基础研究人才储备。这些人熟悉RNA相关的很多技术平台和操作,哪怕不是做药的,随着药物发展的推进,会有很多人从科研界进入到RNA药物的研发上来。另一方面,虽然mRNA药物较少,但此领域的很多人只要有兴趣投入到这个方向,转进来适应一段时间,也有相当多的人才会快速融入,为行业发展带来动力。因此,长期而言,在政府和企业的双方努力下,人才缺乏的问题会逐渐得到解决。
虽然目前国内mRNA领域有所降温,但据相关投资人士来看,该行业依旧炙手可热,一些投资机构仍在寻找好的目标。眼下,后入局者依旧颇多,不少企业仍揣着门票等着进入mRNA行业,因为mRNA技术确实具有非常潜力化的优势。
其一、mRNA技术自身的优势。mRNA疫苗不需进入细胞核也不会参与DNA结构改造,因而机理更简单、安全;mRNA药物设计只需要病毒的基因序列,所以成本更低;同时mRNA属于人体细胞内自有物质,可以自然降解无代谢毒性。
其二、mRNA技术的适应症拓展。Nature也预计到2035年,mRNA市场规模会攀升到230亿美元,新冠疫苗的比例下降到22%,治疗性疫苗比例会达到32%,其他感染性疾病mRNA疫苗比例占到30%,治疗性mRNA药物比例约为16%。
与此同时,国内走在前面的公司,也已经在继续探索新冠疫苗后的下一个mRNA赛道:艾博生物与沃森生物还将合作开发带状疱疹mRNA疫苗、斯微生物的mRNA个性化肿瘤疫苗也进入海外临床阶段。
这次新冠疫情,既从技术上推动了mRNA相关技术的平台能力建设,也从企业经营、国际地位等方面推动了疫苗行业的发展。即便是如今mRNA疫苗市场暂时放缓,但仍有大量企业布局了mRNA疗法。虽然国外吃到了疫情的第一口“蛋糕”,但随着国内mRNA技术的不断革新和发展、防疫政策的放开、适应症的拓展、国内第一款mRNA疫苗的上市,这些都将使得国内mRNA疗法有着可期的巨大市场前景,我们可以期待2021年冷下来的国内mRNA市场在未来能再度迎来热度。
来源:星耀研究院


{replyUser1} 回复 {replyUser2}:{content}