提高抗癌能力!《自然》发现免疫疗法的“逆向”升级关键
利用抗体治疗癌症,这一概念在过去几年中已经在某些类型的癌症中取得了令人振奋的成功。经过设计,一些抗体能选择性地靶向癌细胞表面特有的抗原,从而与癌细胞紧密结合,以便机体的免疫系统前来摧毁这些癌细胞。
抗体与其靶标相结合的紧密程度被称为“亲和力”。当前,用于筛选治疗性抗体的方法通常将高亲和力作为选择的关键标准。然而,日前发表在顶尖学术期刊《自然》上的一项研究却发现,降低亲和力而不是提高亲和力,反而可以让一类治疗性抗体的抗肿瘤活性变得更强,更有效地治疗癌症。

这类治疗性抗体统称为激动型抗体,并非直接靶向肿瘤细胞上的抗原,而是靶向免疫细胞上的受体,如TNF受体CD40、4-1BB等。它们通过改变免疫细胞内的信号传导,促使免疫细胞有更强的抗癌活性,也被称为免疫调节抗体。
与直接靶向抗体相比,激动型抗体的活性规则更为复杂,由抗体表位、亚型和Fcγ受体需求的组合决定。在此次研究中,南安普敦大学癌症免疫学中心的科研团队以三种独立的典型靶标受体为例,系统性地研究了亲和力对激动型抗体活性的影响。
▲激动型抗体结合并激活受体(图片来源:南安普顿大学)
首先,以CD40为范例,研究作者生产了一组抗CD40抗体的亲和力突变体。一系列体内和体外实验显示,与高亲和力的亲本抗体相比,亲和力较低的突变体具有更高的活性,例如提高了B细胞CD23和CD86的表达和细胞增殖。在小鼠体内,这种更高水平的激动活性促进了特异性T细胞的增殖并且可以转化为有效的抗肿瘤活性,对肿瘤细胞有更强的杀伤力。
与之相似的是针对TNF受体家族的共刺激受体4-1BB,研究人员以已经进入临床试验阶段的人源化单抗utomilumab为基础,生产了一组低亲和力的变体,同样发现相比高亲和力亲本抗体,低亲和力utomilumab变体能够在独立于Fcγ受体的系统中诱导显著的T细胞活性并诱导4-1BB受体聚集。这些数据显示,低亲和力效应并不限于CD40,在TNF受体家族成员中普遍适用。
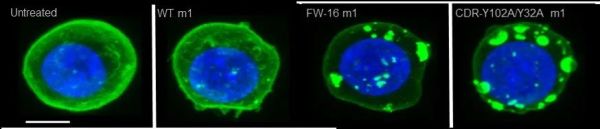
▲荧光显微镜下可以观察到,低亲和力抗体能诱导更高水平的CD40受体聚集(图片来源:参考资料[1])
不仅如此,研究作者把范围拓展到TNF受体家族以外,考察了另一个重要的癌症免疫疗法靶点:PD-1受体。阻断PD-1信号的抗体能够使耗尽的T细胞恢复活力,已经被批准在临床治疗多种癌症。除了癌症,用于诱导PD-1信号的激动型抗体在临床前模型中显示,还可以通过抑制自身反应性T细胞的活化来治疗自身免疫疾病。
作者选择了已获批临床使用的PD-1抑制剂nivolumab并生产了一组低亲和力变体。实验结果再次表明,与CD40和4-1BB相似,低亲和力能够诱导PD-1信号传导。低亲和力PD-1抗体通过增强PD-1受体聚集去有效诱导人源T细胞的PD-1信号传导和抑制T细胞活化。
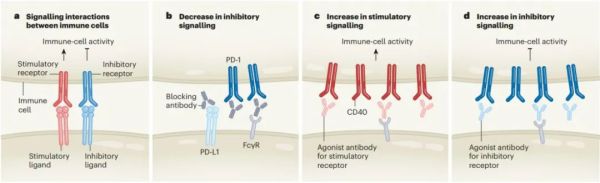
▲治疗性抗体与受体结合的紧密程度影响抗体的有效性(图片来源:参考资料[2])
该论文的第一作者俞晓杰博士(现就职于西湖大学生命科学学院任助理教授)指出:“高亲和力一直是治疗性抗体开发的一个必要条件,所以低亲和力抗体具有更好的活性是个意想不到的发现。”
而这一发现揭示了操纵治疗性抗体活性的新范式,研究人员将此总结为“通过放松抓握使抗体变得更有效”,即改变抗体与受体结合的紧密性将抗体微调到所需的水平和活性,最终为治疗疾病提供了一种高效且高度灵活的途径。
论文通讯作者、南安普顿大学癌症免疫学中心的Mark Cragg教授说:“尽管批准的抗体药物数量在不断增加,目前已有100多种药物获得批准,但许多患者仍然没有反应或对治疗产生耐药性。因此,开发新的策略,通过亲和工程等技术为我们的抗体充电,是为患者提供更好治疗的关键。”
来源:药明康德
版权及免责声明:本网站所有文章除标明原创外,均来自网络。登载本文的目的为传播行业信息,内容仅供参考,如有侵权请联系答魔删除。文章版权归原作者及原出处所有。本网拥有对此声明的最终解释权。


{replyUser1} 回复 {replyUser2}:{content}