近日,猎药人网站(drughunter.com)发布了2022年度小分子榜单,这些分子是从数以万计的研究论文中挑选出来的,并根据读者和审评人的提名情况敲定最终的入围分子。根据猎药人网站的介绍,入围的分子主要为2022年首次披露的分子,或是在临床研发、监管、商业交易等方面有重大进展的分子。
▲Deucravacitinib结构式(图片来源:PubChem)
百时美施贵宝(BMS)公司开发的deucravacitinib(商品名:Sotyktu)是一种口服、选择性酪氨酸激酶2(TYK2)别构抑制剂。Deucravacitinib的靶点TYK2是Janus激酶家族(JAKs)的成员之一,参与调节了多种促炎细胞因子(如IL-12、IL-23和I型干扰素)的相关信号通路,deucravacitinib通过与TYK2的调节性结构域相结合,将TYK2“锁定”在失活的状态,从而选择性抑制TYK2的活性。FDA于2022年9月批准其用于治疗中重度银屑病成人患者,这是近10年来首个针对该适应症的新型口服疗法,并且也是FDA批准的首款TYK2抑制剂。在临床试验中,经过60周的治疗后,近六成中重度斑块型银屑病患者(58.7%)的皮肤症状几乎完全清除。此外,deucravacitinib也代表着新药开发方面的两项突破:它是在药物设计过程中,首款有意使用氘代手段的获批新药;同时它还是首款获得批准,通过靶向结合假激酶(pseudokinase)蛋白域抑制激酶活性的别构抑制剂。▲MRTX1133结构式(图片来源:PubChem)
Mirati公司开发的MRTX1133是一款非共价抑制剂,可以与KRAS G12D的失活和激活状态结合,抑制其的活性。它对KRAS G12D具有高度选择性,对该突变的选择性是野生型KRAS的1000倍以上。在多种携带KRAS G12D基因突变的动物模型中,MRTX1133显著减小了肿瘤大小,尤其是在胰腺癌肿瘤模型中。实验结果显示,经过MRTX1133治疗后,11个胰腺癌模型中有8个(73%)显示出肿瘤缩小超过30%。此外,MRTX1133还入围了去年“猎药人”年度小分子榜单,体现了业界对该分子的持续关注度。▲Resmetirom结构式(图片来源:PubChem)
Madrigal Pharmaceuticals开发的resmetirom是一种口服、肝靶向的选择性甲状腺激素受体(THR)-β激动剂。2022年12月和2023年1月,Madrigal公司公布了该分子在治疗非酒精性脂肪性肝炎(NASH)的3期临床试验中获得的积极结果——达成两项肝脏组织学改善终点,并且这两项终点是FDA认为可预测患者临床获益性,并用以支持加速批准治疗带有肝纤维化NASH患者的指标。试验结果显示,resmetirom治疗显著改善了NASH患者的脂肪性肝炎和肝脏纤维化状况。“猎药人”的网站指出,它是NASH治疗领域首个达到3期临床试验主要终点的药物。Madrigal公司预计在2023年上半年提交resmetirom的新药申请(NDA),并寻求加速批准,如果成功获批,它有可能成为几十年来首个被批准用于NASH的新型药物。▲Voxelotor结构式(图片来源:PubChem)
Global Blood Therapeutics(GBT)公司开发的voxelotor(商品名:Oxbryta)是一种能够与靶点形成可逆性共价键的小分子药物,它可以增加血红蛋白对氧的亲和力,并防止血红蛋白聚合,从而达到治疗镰状细胞贫血(SCD)的效果。在其关键性3期临床试验中,接受剂量为1500 mg或900 mg的voxelotor治疗24周后,SCD患者的血红蛋白水平得到了显著持久的改善——血红蛋白水平提高超过1 g/dL的患者比例分别为51.5%(1500 mg)和32.6%(900 mg),显著高于安慰剂组。72周随访分析表明,血红蛋白浓度依旧持续改善,表明该分子有望长期改善SCD患者的症状。Voxelotor于2019年获得FDA的批准,成为可逆性共价药物在慢性适应症中获批的范例。▲Mavacamten结构式(图片来源:PubChem)
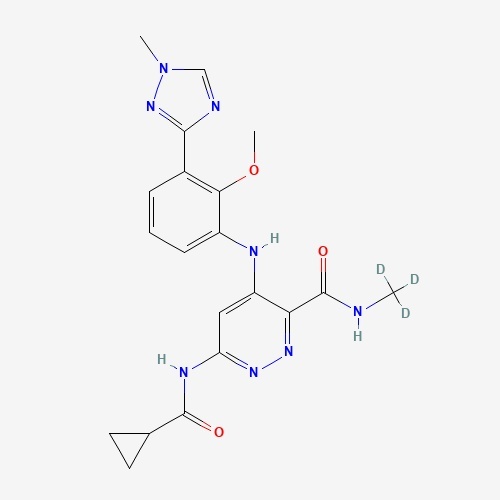
百时美施贵宝(BMS)旗下的mavacamten(商品名:Camzyos)是一种口服、选择性的心肌肌球蛋白别构调节剂。该分子最初由Myokadia公司开发,BMS于2020年以高达131亿美元对其进行收购并将mavacamten纳入其产品管线。Mavacamten能将整体肌球蛋白群转变到节能、可募集的超松弛状态,因此能够减少症状性梗阻性肥厚型心肌病患者的心脏过度收缩症状。在临床期和临床前研究中,mavacamten可以降低心壁应激的生物标志物,减轻过度的心肌收缩力,减少左心室流出道梯度和增加舒张顺应性。2022年,mavacamten被FDA批准用于治疗成人梗阻性肥厚型心肌病,成为了FDA批准的首款心肌肌球蛋白别构可逆性抑制剂。Kura Oncology的口服menin-MLL1抑制剂
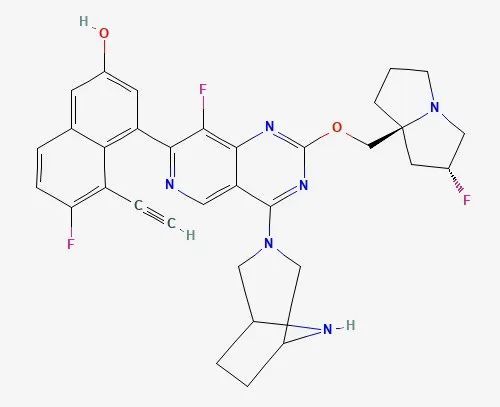
▲Ziftomenib结构式(图片来源:PubChem)
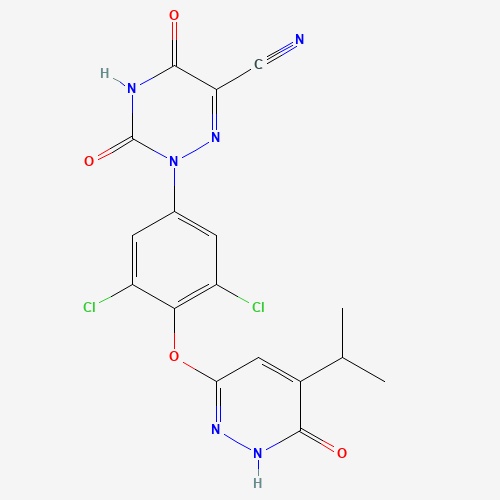
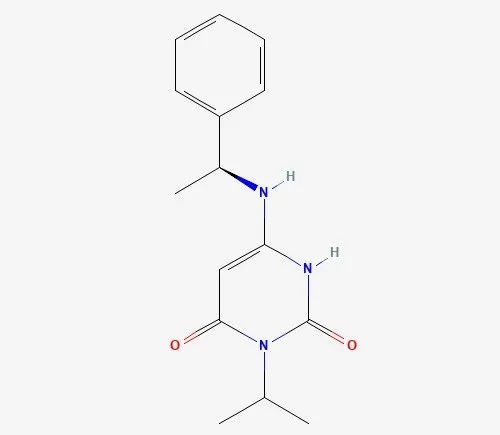
Ziftomenib(KO-539)是Kura Oncology公司为急性髓系白血病(AML)患者开发的口服小分子抑制剂,它可以抑制menin和MLL1蛋白之间的相互作用,两者之间的相互作用是许多白血病的驱动因素。在早期临床试验中,接受600 mg剂量ziftomenib的20例NPM1突变型AML患者中有30%达到了完全缓解,并且安全性和耐受性良好。目前该药物的2期试验已完成了首批患者给药。▲LP0200结构式(图片来源:参考资料[1])
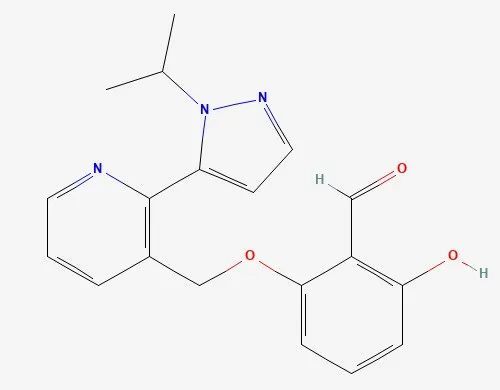
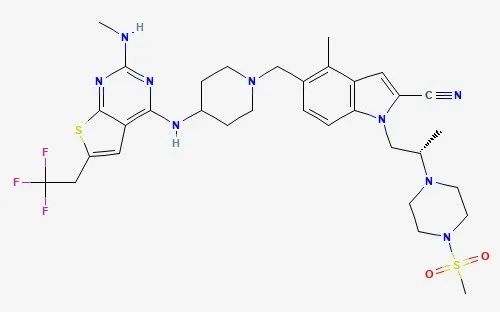
IL-17一直是免疫学中的热门靶点,它与包括银屑病、银屑病关节炎和强直性脊柱炎在内的多种免疫性疾病相关。LEO Pharma的在研银屑病疗法LP0200是一款针对IL-17的小分子拮抗剂,靶向作用于IL-17的同源二聚体,可防止IL-17与其受体相互作用。2022年8月,LEO Pharma完成了LP0200的1期临床研究,该研究是在健康的志愿者中评估该化合物的安全性。不过,LEO Pharma公司在2022年度报告中也指出,由于试验中展现的一些特性并不尽如人意,该公司已将研究重点转移到其他的备选化合物。▲YCT529结构式(图片来源:PubChem)
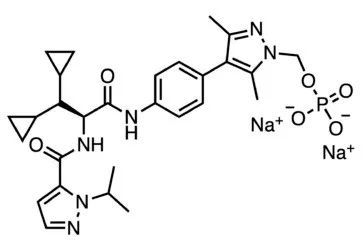
YourChoice Therapeutics公司开发的YCT529是一种潜在的非激素男性避孕药,可作为视黄酸受体α(RAR-α)的选择性拮抗剂。在临床前研究中,该分子显著减少了小鼠的精子产量,其预防怀孕的成功率高达99%,并且没有在动物模型中观察到明显的毒副作用。如果它对人类也同样安全有效,那么它有望为男性提供新的避孕选择。该分子预计将于2023年上半年进入临床开发。▲Emraclidine的结构式(图片来源:PubChem)
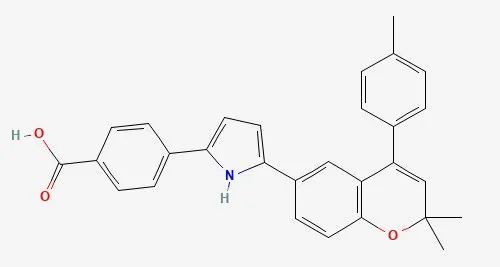
Cerevel Therapeutics开发的emraclidine(CVL-231)是一款毒蕈碱M4选择性正变构调节剂(PAM)。在动物模型研究中,该分子显示出高度的脑渗透性,并且在PET研究中表现出较好的靶点参与情况。去年12月,Cerevel公司公布了该药物用于精神分裂症成人患者的早期临床数据。结果显示,与安慰剂相比,emraclidine在阳性和阴性症状量表(PANSS)总分中显示出具有临床意义和统计学意义的改善,总体耐受性良好。动态血压监测试验结果显示,emraclidine长期给药不会引起精神分裂症患者血压升高。同时,研究结果还表明,选择性靶向M4毒蕈碱受体亚型是治疗精神分裂症的潜在新方法。▲Avacopan的结构式(图片来源:PubChem)
Avacopan是一款口服选择性补体5a(C5a)受体抑制剂,最初由ChemoCentryx公司开发,安进(Amgen)在2022年对该公司进行收购并将该分子纳入自身产品管线。Avacopan通过精确阻断位于中性粒细胞等炎症细胞上的C5a受体,阻止这些细胞受到C5a的激活,降低炎症损伤。在3期临床试验中,该药物显著改善了多血管炎和肉芽肿伴多血管炎患者的症状,具体而言,在治疗第52周,avacopan组有65.7%的患者观察到持续缓解,对照药物组为54.9%(非劣效性P<0.001;优效性P=0.007)。2021年10月,FDA批准了avacopan的上市申请,与标准疗法联用,辅助治疗两种主要的抗中性粒细胞胞浆自身抗体(ANCA)相关血管炎:显微镜下多血管炎(MPA)和肉芽肿伴多血管炎(GPA)。ChemoCentryx公司在新闻稿中指出,这是十年来,FDA首次批准ANCA相关血管炎药物,也是FDA批准的首款口服补体C5a受体抑制剂。



{replyUser1} 回复 {replyUser2}:{content}