开发“first-in-class”药物的关键——近期那些靶点值得关注?
《自然》子刊Nature Reviews Drug Discovery曾指出,每个“first-in-class”药物的上市多有赖于创新、有效药物靶点的发现,而这也是驱动疾病疗法产生根本性突破的源头。药明康德内容团队检视今年6月发布于国际知名科学期刊的研究,整理了具转化潜力的多项潜在新药靶点,供生物医学产业作为创新研发的参考。限于篇幅,仅针对部分潜在靶点进行介绍。
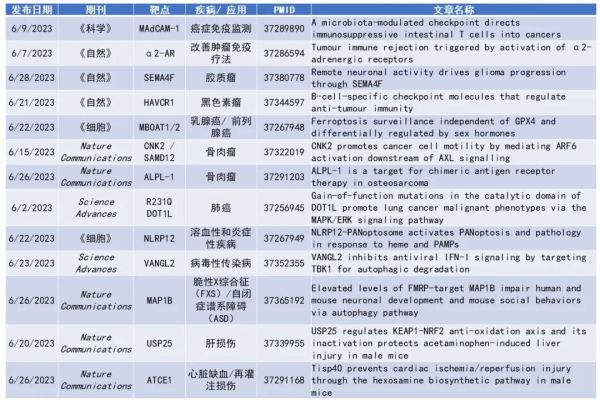
药明康德内容团队整理
靶点:MAdCAM-1
应用:癌症免疫监测
期刊/PMID:《科学》/ 37289890
发现:已过发现当癌症病患在接受免疫检查点阻断(ICB)疗法治疗前使用抗生素,然后在治疗开始前停药时,会导致免疫检查点阻断疗法的疗效降低,因此有假说认为患者体内的细菌可能影响其治疗反应。在此研究中,科学发现接受抗生素治疗后的小鼠肠道内肠梭菌(Enterocloster species)的重新定植会导致整合素α4β7配体MAdCAM-1的表达下调。由于MAdCAM-1有助于T细胞(Tr17细胞)的免疫抑制亚群保留在肠道中,因此其表达下调会导致Tr17细胞转移到肿瘤和肿瘤引流淋巴结,进而降低免疫检查点阻断治疗的疗效。此外,研究人员还发现在接受免疫治疗的肾、膀胱和肺癌患者中,其血液中可溶性MAdCAM-1的低水平与其肠道微生物群失调以及患者不良的临床结局相关。因此调控癌症患者体内或肠道中MAdCAM-1水平有望改善免疫疗法在这类癌症患者的疗效。
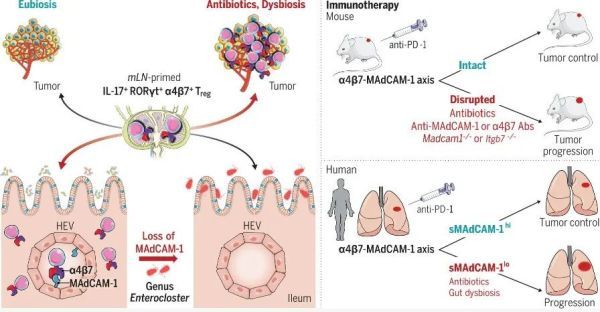
▲MAdCAM-1为癌症免疫监测的肠道免疫检查点(图片来源:参考资料[1])
靶点:α2-AR
应用:改善肿瘤免疫疗法
期刊/PMID:《自然》/ 37286594
发现:免疫检查点阻断疗法作为单药治疗癌症患者的效果通常不理想,因此常需要通过与其他化合物作为组合疗法来使用,这些化合物能够降低肿瘤微环境中的免疫抑制。科学家发现,α2-肾上腺素能受体(α2-AR)激动剂作为单药治疗时,在多种免疫活性肿瘤模型(包括ICB耐药模型)中具有非常强的抗肿瘤活性,但在免疫缺陷模型中则没有。当科学家使用α2-AR拮抗剂或敲除小鼠的Adra2a基因(编码α2a-AR)时,α2-AR激动剂的抗肿瘤作用会被逆转,显示激动剂靶向宿主细胞而非肿瘤细胞。此外,接受治疗的小鼠肿瘤中浸润的T淋巴细胞增加,髓系抑制细胞则凋亡、减少。单细胞RNA测序分析发现巨噬细胞和T细胞中的先天和适应性免疫反应通路产生上调。在Adra2a敲除小鼠中的研究显示,激动剂直接作用于巨噬细胞,增加其活化T淋巴细胞的能力。因此靶向α2-AR的激动剂或可提高癌症免疫治疗的临床疗效。
靶点:MBOAT1/2
应用:乳腺癌/前列腺癌
期刊/PMID:《细胞》/ 37267948
发现:铁死亡(ferroptosis)是由铁依赖性磷脂过氧化作用所驱动的细胞死亡过程,与多种疾病有关。抑制铁死亡主要有两种监测机制:一种由催化磷脂过氧化物还原的谷胱甘肽过氧化物酶4(GPX4)介导,另一种由产生具有自由基捕获抗氧化活性代谢物的酶(如FSP1)介导。在这项研究中,科学家通过全基因组CRISPR筛选与后续机制研究发现,磷脂修饰酶MBOAT1和MBOAT2是铁死亡的抑制因子。MBOAT1/2通过重塑细胞磷脂谱来抑制铁死亡,且其铁死亡监测功能独立于GPX4或FSP1。MBOAT1和MBOAT2分别受雌激素受体(ER)和雄激素受体(AR)控制转录上调。科学家发现ER或AR拮抗剂加上诱导铁死亡的组合疗法可显著抑制ER+乳腺癌和AR+前列腺癌的生长,即使肿瘤对单药激素治疗具耐药性亦然。
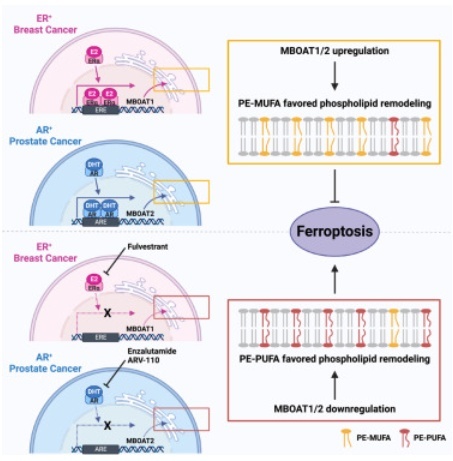
▲抑制MBOAT1/2促进铁死亡(图片来源:参考资料[3])
靶点:ALPL-1
应用:骨肉瘤(CAR-T疗法靶点)
期刊/PMID:Nature Communications / 37291203
发现:骨肉瘤(OS)多发生与儿童和年轻成人中,其中转移性和复发性肿瘤患者的结局较差。由于肿瘤内异质性和潜在靶向蛋白的大量脱靶表达,与其他癌症类型相较,免疫治疗对于OS患者的疗效有限。在此研究中,科学家开发了靶向一种碱性磷酸酶亚型ALPL-1的嵌合抗原受体(CAR)T细胞。ALPL-1在原发性和转移性OS中皆具高度且具特异性地表达。实验证实,这类CAR-T细胞可在体外,以及原发性和转移性OS的原位小鼠模型中,有效介导对ALPL阳性细胞的细胞毒性,并且对造血干细胞或健康组织不产生不在预期中的毒性。
靶点:VANGL2
应用:病毒性传染病
期刊/PMID:Science Advances / 37352355
发现:严格控制1型干扰素(IFN-I)信号是对抗病毒感染产生强效先天性免疫应答的关键,然而其潜在的分子机制仍不明确。科学家发现在水泡性口炎病毒(VSV)感染过程中,VANGL2蛋白为一IFN诱导的负反馈调节因子,可抑制IFN-I信号。小鼠髓样细胞VANGL2的特异性缺失会增强抵抗VSV感染的IFN-I信号,提升小鼠存活率。这些发现显示靶向VANGL2可能是治疗病毒感染性疾病的潜在临床靶点。
靶点:MAP1B
应用:脆性X综合征(FXS)/自闭症谱系障碍(ASD)
期刊/PMID:Nature Communications / 37365192
发现:在此篇研究中,研究人员发现脆性X信使核糖核蛋白1蛋白(FMRP)的缺乏会导致发育中的人和非人灵长类皮层神经元微管相关蛋白1B(MAP1B)升高。当健康人类神经元中MAP1B基因的激活或自闭症谱系障碍(ASD)患者神经元中MAP1B基因的三倍化,皆会抑制个体的形态和生理成熟。实验显示,成年雄性小鼠前额叶皮质兴奋性神经元Map1b的激活会损害其社会行为能力。当敲除MAP1B基因时,可逆转离体ASD和FXS患者人脑组织中,因缺乏FMRP而导致的神经元缺陷。因此靶向MAP1B可能是治疗FXS和ASD患者的潜在靶点。
靶点:USP25
应用:肝损伤
期刊/PMID:Nature Communications / 37339955
发现:核因子红系2相关因子2(NRF2)是一种负责启动抗氧化基因表达程序,以对抗氧化应激反应的转录因子。在非应激条件下,CUL3 E3泛素连接酶的接头蛋白KEAP1介导NRF2的泛素化和降解。研究人员发现去泛素化酶USP25可直接与KEAP1结合,阻止KEAP1自身的泛素化和降解。在没有Usp25或去泛素化酶被抑制的情况下,KEAP1的表达下调,进而使得NRF2水平保持稳定,使细胞更容易对氧化应激作出反应。在对乙酰氨基酚(APAP)过量诱导的氧化性肝损伤雄性小鼠模型中,无论是在遗传学还是药理学上抑制Usp25,都大大降低小鼠的肝损伤,进而降低致死剂量APAP导致的死亡。
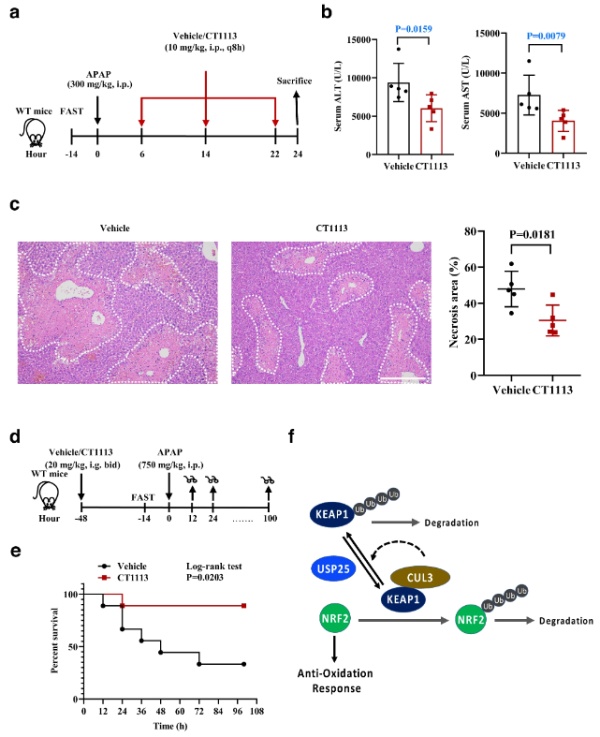
▲抑制USP25降低小鼠因过量乙酰氨基酚造成的肝损伤(图片来源:参考资料[7])
来源:药明康德
版权及免责声明:本网站所有文章除标明原创外,均来自网络。登载本文的目的为传播行业信息,内容仅供参考,如有侵权请联系答魔删除。文章版权归原作者及原出处所有。本网拥有对此声明的最终解释权。


{replyUser1} 回复 {replyUser2}:{content}