总缓解率94%的CAR-T疗法、治疗阿尔茨海默病的NK细胞疗法...
1. 同种异体CAR-T细胞疗法CB-010治疗复发/难治性B细胞非霍奇金淋巴瘤患者的疗效亮眼,患者的总缓解率(ORR)为94%,最长保持了24个月的完全缓解(CR)。
2. 用于治疗活动性甲状腺眼病(TED)的在研新药VRDN-001可使慢性TED患者的症状和体征在第6周就得到快速且有临床意义的改善。3. NKGen Biotech公司公布了其用于治疗阿尔茨海默病的自然杀伤(NK)细胞疗法SNK01在1期临床试验中的积极中期数据。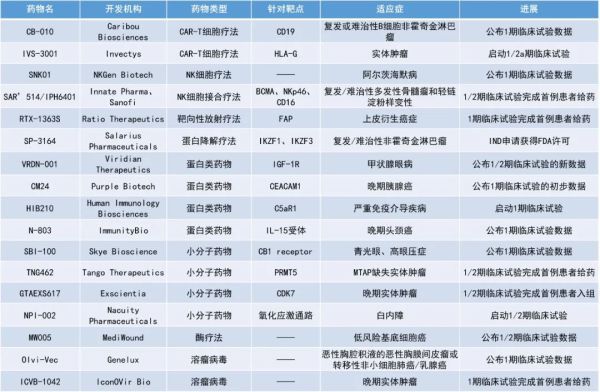
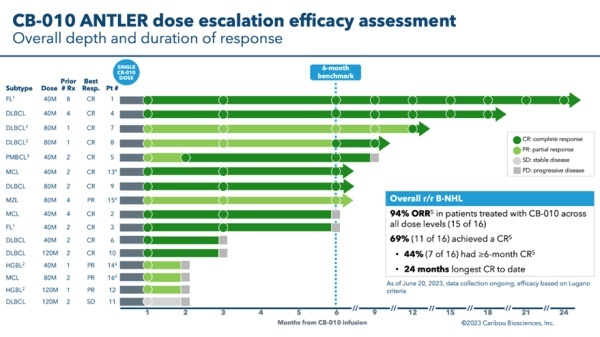
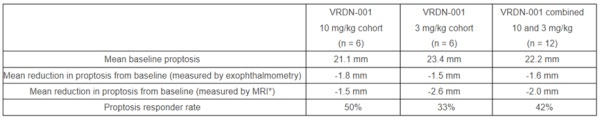
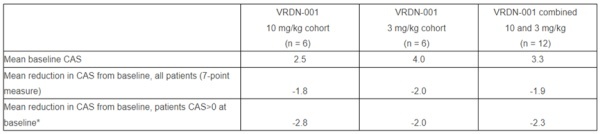
Caribou Biosciences公司公布了其同种异体CAR-T细胞疗法CB-010治疗复发/难治性B细胞非霍奇金淋巴瘤患者的长期随访数据。CB-010利用基因编辑技术生成,除了表达靶向CD19的嵌合抗原受体,还利用基因编辑技术敲除了免疫检查点蛋白PD-1的表达,旨在提高抗肿瘤活性的持久性。此次公布的结果显示,CB-010的缓解率和安全性可与已获批的自体CAR-T细胞疗法相媲美。接受单剂CB-010治疗后,患者的ORR为94%(15/16),CR率为69%(11/16),44%的患者保持CR超过6个月。截至目前,患者最长保持了24个月的CR。大B细胞淋巴瘤患者亚组中有50%的患者保持CR超过6个月,患者最长保持了18个月的CR.▲CB-010的疗效评估图(图片来源:参考资料[15])VRDN-001是Viridian Therapeutics公司开发的一种用于治疗TED的抗IGF-1R单克隆抗体,可以通过亚纳摩尔级别的亲和力结合和阻断IGF-1R信号通路。这种作用机制已在TED的临床实践中得到了验证。此次公布的数据来自一项双盲、安慰剂对照的临床1/2期试验中3 mg/kg和10 mg/kg VRDN-001剂量队列的数据。结果显示,两种剂量的VRDN-001都能使慢性TED患者的眼球突出程度和临床活动评分(CAS)在第6周得到快速且有临床意义的改善,如下图所示。此外,VRDN-001在所有剂量下均显示出了良好的安全性。NKGen Biotech公司公布了其NK细胞疗法SNK01治疗阿尔茨海默病患者的1期临床试验数据。截至2023年6月30日的数据,SNK01在10名中位年龄为79岁的受试者中耐受性良好,未观察到相关严重不良事件,也未达到剂量限制性毒性。第11周(末次给药后一周)时,70%的受试者CDR-SB评分(分越高意味着患者临床功能越低)保持稳定或有改善,60%的受试者的ADAS-Cog评分(用于评估认知能力)保持稳定或有改善,50%的受试者的MMSE评分(用于评估精神状态)保持稳定或有改善。一名接受最高剂量水平治疗的受试者的MMSE评分(从14分提升至22分)、ADAS-Cog评分(从32分降低到24分)和CDR-SB评分(从10分降低到5.5分)均有显著改善。此外,观察到受试者脑脊液中的生物标志物水平保持稳定或有改善,在停止SNK01治疗3个月后,一些生物标志物出现了反弹。第22周(末次给药后3个月)时,8名可评估的受试者中,67%的受试者的CDR-SB评分保持稳定,83%的患者的ADAS-Cog评分和MMSE评分保持稳定或有改善。SP-3164是Salarius Pharmaceuticals公司开发的分子胶类蛋白降解剂,通过诱导E3泛素连接酶和靶蛋白之间的相互作用,能够选择性地降解靶蛋白。在临床前研究中,SP-3164能够降解转录因子IKZF1和IKZF3蛋白,故而具有抗癌和免疫调节的特性。此外,SP-3164在滤泡性淋巴瘤和多发性骨髓瘤动物模型中显示出令人信服的抗肿瘤活性。近期,FDA批准了SP-3164的IND申请,允许该公司在复发/难治性非霍奇金淋巴瘤患者中进行SP-3164的1期临床试验,以评估其安全性、临床活性、药代动力学和药效学。Purple Biotech公司公布了其靶向CEACAM1的单克隆抗体CM24联用PD-1抑制剂nivolumab治疗晚期胰腺癌患者的初步临床数据。CEACAM1是一种免疫检查点蛋白,可通过多种途径支持肿瘤免疫逃逸和存活。NET是一种网状DNA结构,覆盖着由活化的中性粒细胞释放的致癌蛋白,已被证明可包裹肿瘤并促进免疫逃避、肿瘤进展和转移。当CEACAM1与NET结合时,它将成为癌症细胞粘附的重要位点,因此被认为是预防肿瘤转移进展和免疫逃逸的潜在治疗靶点。在临床前研究中,CM24已被证明可直接与NET结合,并抑制NET诱导的癌症细胞迁移。此次研究招募了11名难治性胰腺导管腺癌患者,这些患者在接受了2线治疗后进展。该联合疗法在所有剂量水平下的耐受性均良好,无药物限制性毒性。6例患者出现3级不良反应,但均与研究药物无关。初步的疗效结果显示,接受CM24联合nivolumab治疗的患者的总生存期与三线治疗为化疗的患者的历史总生存期相当,接受化疗患者的中位总生存期为3-4个月。ImmunityBio公司公布了其IL-15超级拮抗剂N-803联合同种异体细胞因子诱导记忆样(CIML)NK细胞治疗晚期头颈癌患者的1期临床试验结果。N-803由与IL-15受体α/IgG1 Fc融合蛋白结合的IL-15突变体(IL-15N72D)组成。它与βγT细胞受体结合,能够直接特异性刺激CD8阳性T细胞和NK细胞,同时避免刺激调节性T细胞。与天然、非复合IL-15相比,N-803在患者体内具有更优的药代动力学特性,且能在淋巴组织中存在更长时间,表现出增强的抗肿瘤活性。该研究中,患者在接受同种异体CIML NK细胞疗法联用N-803前接受了清淋治疗加或不加CTLA-4抑制剂ipilimumab治疗。结果显示,患者产生了与持续的CIML NK细胞扩增相关的肿瘤消退。这表明,该联合疗法有望为目前预后极差的晚期头颈癌患者提供新的治疗方法。Skye Bioscience公司公布了其眼用乳剂(OE)SBI-100用于治疗青光眼和眼压增高患者的1期临床试验的最后1个健康受试者队列的数据。SBI-100 OE采用新型分子结构和纳米乳剂配方,使其中的有效成分CB1R激动剂可更好地穿透眼内组织,实现有效的局部给药,对降低眼内压具有良好的疗效。此次公布的数据显示,SBI-100 OE的耐受性良好,与先前报告的5个队列一致,没有与药物相关的严重不良事件。该公司准备在2023年第3季度将SBI-100 OE推进至针对青光眼患者的2a期临床试验。MediWound公司公布了其酶疗法MW005治疗低风险基底细胞癌的安全性和有效性数据。15名患者接受了MW005治疗并完成了研究。结果显示,MW005的安全性和耐受性良好,患者依从性高。尽管该试验的主要重点是安全性和耐受性,但值得注意的是,根据临床评估,15名患者中有11名实现了基底细胞癌的完全清除,其中,大多数患者经组织学证实实现了完全清除。Genelux Corporation公司公布了其溶瘤病毒免疫疗法Olvi-Vec治疗恶性胸腔积液的恶性胸膜间皮瘤或转移性非小细胞肺癌/乳腺癌患者的1期临床试验结果。Olvi-Vec是Genelux公司专有的溶瘤病毒疫苗,经过改良以提高其安全性、肿瘤选择性和治疗潜力。此次公布的结果表明,Olvi-Vec可感染肿瘤细胞,同时降低肿瘤细胞密度,增加免疫细胞密度,证实了Olvi-Vec具有直接的细胞毒性和免疫激活作用。所有患者的中位总生存期为19.5个月,恶性胸膜间皮瘤亚组患者的中位总生存期为22个月。试验中没有出现剂量限制性毒性反应或需要减少剂量,也没有达到最大耐受剂量。因此,推荐剂量尚未确定。






{replyUser1} 回复 {replyUser2}:{content}