研发投入最多的十家药企,它们看好哪些寡核苷酸疗法?
本系列讨论的新分子疗法涵盖了寡核苷酸疗法(包括RNA疗法、反义寡核苷酸等)、细胞和基因疗法、蛋白降解疗法、多特异性抗体,以及抗体偶联药物(ADC)。这些创新疗法各有其独特之处,它们的出现从根本上颠覆了传统治疗的范式。为了更系统地呈现这些信息,我们将内容分为四篇,与读者逐一分享。在今天的内容中,我们将详细盘点寡核苷酸疗法领域的最新研发进展。
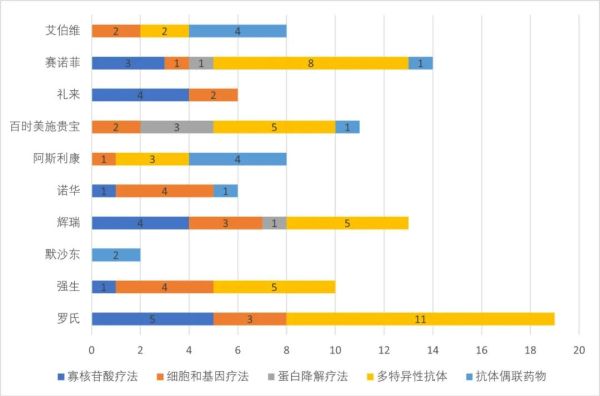
▲2022年研发投入最多的十家药企新分子疗法管线布局(药明康德内容团队制图)
寡核苷酸疗法是一类基于短核苷酸序列的新颖治疗模式,它们作用于基因转录和翻译的过程,旨在调节细胞中特定RNA或DNA分子的表达或功能。这种治疗方法通常针对遗传突变,或在RNA水平上调节基因的表达。它具有调节以前被认为“不可成药”的靶点的潜力,并且因其快速的临床开发周期而备受关注。
常见的寡核苷酸疗法主要有以下几种类型:反义寡核苷酸(ASO)、小干扰RNA(siRNA)、微小RNA(miRNA)、核酸适配体(Aptamer)以及诱饵寡核苷酸(Decoy ODN)等,这种创新治疗模式在治疗遗传疾病、癌症和传染病方面展现出了巨大的潜力。例如,可以通过设计特定的寡核苷酸,针对遗传疾病中的突变RNA分子,从而关闭或修复异常的基因表达。随着技术的进步,寡核苷酸疗法也已被引入到如非酒精性脂肪性肝炎和心血管疾病等常见慢性疾病的治疗中。
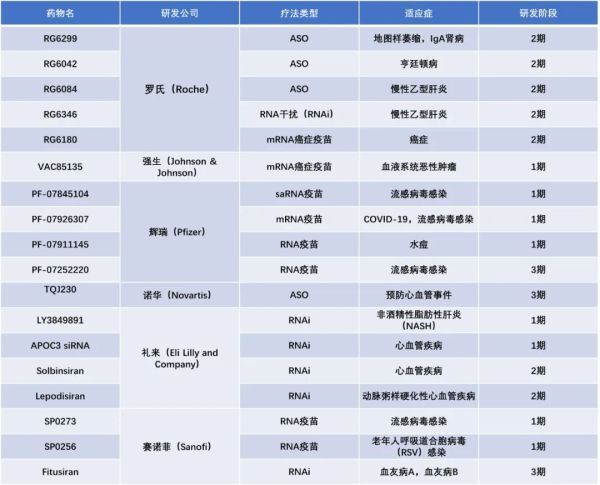
▲2022年研发投入最多的十家药企旗下在研寡核苷酸疗法(药明康德内容团队制图)
反义寡核苷酸(ASO)
候选药物:RG6299(IONIS-FB-LRx)
IONIS-FB-LRx是罗氏和Ionis Pharmaceuticals共同开发的反义寡核苷酸药物,可以减少补体先天免疫系统中关键蛋白FB的产生。FB主要在肝脏中产生,并在整个血液系统中循环,包括眼睛和肾脏中的血管。该补体蛋白在先天免疫原性级联反应中起关键作用,这一级联反应的过度活化,与多种补体介导疾病的发病有关。
IONIS-FB-LRx目前正处于2期临床研究阶段,在针对IgA肾病的试验中,IONIS-FB-LRx达到了24小时尿蛋白变化的主要终点:从基线时到治疗第29周,患者的蛋白尿平均减少了44%。研究中所有患者的肾功能(以估算肾小球滤过率衡量)均保持不变,IONIS-FB-LRx还使血浆补体因子B(CFB)、替代途径活性(AH50)和尿液补体因子Ba(因子Ba)实现了显著且持续的降低。在这项研究中,IONIS-FB-LRx表现出了良好的安全性和耐受性。
候选药物:RG6042(tominersen)
Tominersen也是罗氏和Ionis公司合作开发的一种ASO疗法,拟开发治疗亨廷顿病(HD)。亨廷顿病是一种遗传性神经退行性疾病。突变的亨廷顿蛋白具有神经毒性,致使大脑中的神经细胞逐渐受损死亡,患者的智力和身体控制能力发生越来越严重的退化。作为一款反义ASO疗法,tominersen可以通过减少亨廷顿蛋白的产生,达到治疗亨廷顿病的目的。目前,tominersen处于2期临床研究阶段。
候选药物:RG6084(RO7191863)
RG6084是是罗氏开发的一种肝脏指向性的单链寡核苷酸,靶向PD-L1的mRNA,用于乙肝治疗。临床前概念研究显示,RO7191863能够有效结合靶标,扩增肝脏内CD4+/CD8+T细胞、NK细胞及抗原提呈细胞水平,诱导剂量依赖性抗病毒应答。
在2021年11月举行的美国肝病研究学会年会(AASLD 2021)上,罗氏首次公布了RO7191863的1期临床研究结果。该研究入组的对象为接受稳定抗病毒治疗且无明显肝纤维化证据的病毒学抑制慢性乙肝患者,初步的安全性和有效性数据表明,通过肝脏定向抑制PD-1/PD-L1的mRNA表达,进而来靶向PD-1/PD-L1通路是可行的,并支持RG6084与其它疗法联合用药,以实现对慢性HBV感染患者的功能性治愈。
目前,RG6084在治疗慢性乙型肝炎感染患者的2期临床研究中进行测试。
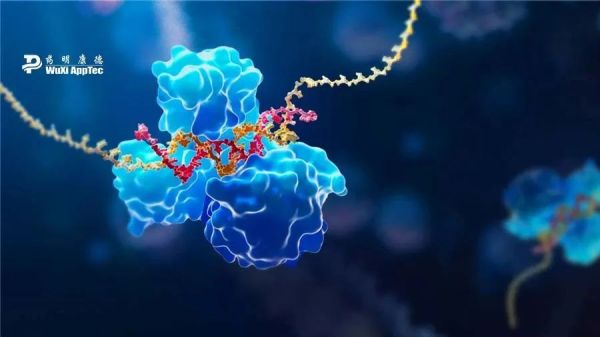
候选药物:TQJ230(pelacarsen)
TQJ230是由Ionis发现、并于2019年授权给诺华进行全球独家开发、生产和商业化的在研ASO疗法。它通过降解编码Lp(a)的mRNA以降低肝脏中Lp(a)的表达水平。此前公布的2b期临床试验数据显示,98%的患者在接受pelacarsen治疗后,Lp(a)水平降低到50 mg/dL以下,这是降低心血管疾病风险的阈值。
Pelacarsen目前正在Lp(a)HORIZON试验中进行评估,该试验是诺华展开的一项全球性、双盲、安慰剂对照的关键性3期试验。目前,该研究已完成共8323位受试者的入组,预计于2025年会有数据发布。
RNA干扰(RNAi)
候选药物:RG6346(RO7445482)
RG6346(又名RO7445482)是Dicerna公司开发的一款RNAi疗法,拟开发治疗慢性乙肝病毒(HBV)感染。2019年,罗氏与Dicerna公司达成一项14.7亿美元的研发合作与许可协议,共同开发这款创新疗法。
图片来源:123RF
目前乙肝难于治愈的原因是HBV能够在被感染细胞的细胞核中生成共价闭合环状DNA(cccDNA)和整合序列。这些序列的半衰期非常长,目前的标准疗法不能有效清除cccDNA。RG6346能够生成一款靶向HBV基因组特定区域的RNAi,它能够特异性敲低HBV mRNA的生成和HBV进入细胞所需的基因。
2020年11月,Dicerna公司公布了RG6346治疗慢性乙型肝炎的1期临床试验结果。结果显示:每月一次,总计4次的RG6346治疗导致HBV疾病活动生物标志物的大幅和持久降低;最后一次给药后乙肝表面抗原(HBsAg)水平持续降低时间可长达1年。2021年3月,RG6346治疗慢性乙型肝炎病毒感染的2期临床试验正式启动。
图片来源:123RF
候选药物:LY3849891,APOC3 siRNA,solbinsiran,lepodisiran
LY3849891是礼来开发的一款靶向PNPLA3的RNAi疗法,目前正在一项1期临床试验中测试其对具有PNPLA3 I148M基因型的非酒精性脂肪肝炎(NASH)患者中的安全性和耐受性。同时,研究人员还将通过对受试者肝脏进行血液测试和磁共振成像,以确定LY3849891对脂肪性肝病的影响。
APOC3 siRNA,solbinsiran,lepodisiran也是由礼来开发的RNAi疗法,它们都处于1期临床开发阶段。有别于其他专注于遗传性疾病的寡核苷酸疗法,这几款药物所针对的适应症是心血管疾病。目前关于这几种疗法目前公开的信息并不多。
图片来源:123RF
候选药物:fitusiran
Fitusiran是赛诺菲旗下一款基于Alnylam公司的ESC-GalNAc偶联技术,增加皮下注射疗效与持久性的RNAi疗法药物,用以预防性治疗血友病A或B患者,无论这些患者体内是否带有凝血因子抑制物。Fitusiran被设计用以降低抗凝血酶(antithrombin)含量、提升凝血酶生产,以此恢复止血平衡并避免出血。
Fitusiran已进入3期临床开发阶段,根据此前公布的临床数据,与对照组相比,每月一次给药fitusiran(80 mg)预防性治疗显著减少了两种类型血友病患者的出血事件,使年出血率(ABR)降低超过89%,并且改善了患者的生活质量。
图片来源:123RF
mRNA癌症疫苗
候选药物:RG6180(autogene cevumeran)
Autogene cevumeran是由罗氏开发的一款个体化新抗原疫苗。该药物是基于BioNTech的iNeST癌症疫苗技术平台生成的,可以编码数十种新抗原,旨在激发人体针对肿瘤细胞产生更为全面的免疫反应,防止肿瘤细胞逃避免疫系统的攻击。
今年5月,《自然》杂志发表了该疫苗与抗PD-L1抗体atezolizumab和化疗联用治疗胰腺癌的早期临床结果。试验结果显示,这种治疗组合显著推迟接受手术切除的胰腺癌患者的复发时间,凸显了mRNA癌症疫苗的抗癌潜力。此外,该疫苗在试验过程中表现出良好的安全性,并成功诱导出了靶向胰腺癌癌症新抗原的T细胞活性。
目前这款疫苗仍处于2期临床研究阶段。
候选药物:VAC85135
VAC85135是强生旗下杨森(Janssen)公司与Nouscom合作开发的一款新抗原癌症疫苗,基于Nouscom专有的病毒载体平台研制而成。2022年5月,该疫苗的临床试验申请(IND)得到了美国FDA的批准,目前该疫苗正处于1期临床研究中。
图片来源:123RF
预防性RNA疫苗
在寡核苷酸疗法领域,一些公司专注于布局预防性RNA疫苗以对抗多种病毒感染。例如,现阶段辉瑞旗下共有4款RNA疫苗在临床1期研究中进行测试,分别是针对流感的saRNA疫苗PF-07845104,针对COVID-19和流感的mRNA疫苗PF-07926307,可预防水痘-带状疱疹病毒感染的PF-07911145,以及用于流感预防的PF-07252220。目前关于这些疫苗披露的信息不多。
候选药物:SP0273,SP0256
SP0273和SP0256是赛诺菲开发的2种用于预防病毒感染的mRNA疫苗,目前上述2款疫苗正处于1期临床研究阶段,关于这两款疫苗的公开信息不多。

图片来源:123RF
随着医药领域的不断发展,新分子疗法正逐渐引领治疗潮流。在此之中,寡核苷酸疗法以其丰富的候选靶点、短小的研发周期、持久的药效和高的临床开发成功率等多重优势,为许多原本难治的疾病指明了新的治疗方向。特别是在癌症、遗传性疾病以及传染病的治疗领域,该疗法已经取得了显著的进展。
然而,这种疗法也面临一些技术挑战。寡核苷酸由于带有负电荷、分布不均、入胞难度大以及对核酸酶的抗性较低,很容易被降解,这些因素都给它的药物研发增添了难度。
除了上述难题,寡核苷酸疗法的发展还面临着其他亟待解决的问题。大睿生物(Rona Therapeutics)的创始人兼首席执行官史艺宾(Stella Shi)女士曾在药明康德举办的全球论坛中指出,寡核苷酸的规模化生产和成本的降低,以及药物的可负担性都是目前制约寡核苷酸疗法发展的瓶颈。因此,业界需要探索一个先进的生产技术平台来降低成本,并更深入地了解各种内源性RNA的工作原理。

尽管存在挑战,整个行业对寡核苷酸疗法的未来依然持乐观态度,各大药企纷纷在寡核苷酸领域布局研发管线,其中相当一部分疗法已在临床试验中取得了积极结果,未来可期。我们相信,在不远的未来,这种创新疗法将更为广泛地服务于患者,给他们带来健康和希望,并为医疗领域带来创新风潮和无限的可能性。
来源:药明康德
版权及免责声明:本网站所有文章除标明原创外,均来自网络。登载本文的目的为传播行业信息,内容仅供参考,如有侵权请联系答魔删除。文章版权归原作者及原出处所有。本网拥有对此声明的最终解释权。


{replyUser1} 回复 {replyUser2}:{content}