35年长跑!潜在治愈实体瘤,这款细胞疗法迎来关键里程碑
以CAR-T细胞疗法为代表的T细胞疗法在治疗血液癌症领域已经表现出卓越的疗效,让有些患者看到了治愈的希望。然而在治疗实体瘤方面,目前尚未有CAR-T和TCR细胞疗法获得批准。明年年初,一种已有35年历史的细胞疗法有望获得FDA的批准,成为首款获批治疗实体瘤的T细胞疗法,这就是Iovance Biotherapeutics公司开发的肿瘤浸润淋巴细胞(tumor infiltrating lymphocyte,TIL)疗法lifileucel。近日,《自然》子刊Nature Reviews Drug Discovery也发表文章,对TIL疗法的前世今生,以及未来的发展方向进行了回顾和展望。
历史悠久的TIL疗法
TIL是离开血液循环,迁移到肿瘤附近的淋巴细胞。如果把人体免疫系统对癌症的反应比作一场战争,TIL是从身体各处奔往前线,与癌细胞作战的“战士”。它们可以起到杀伤癌细胞的作用。肿瘤中TIL的多少是预测癌症患者预后和对免疫疗法反应的重要指标。
早在1988年,美国国家癌症研究所(NCI)的Steven Rosenberg博士和他的同事们就在《新英格兰医学杂志》上发表论文,展示使用从转移性黑色素瘤组织中分离,在体外通过IL-2刺激培养并增殖的TIL,在注回患者体内后能够为60%的患者带来缓解。在2024年初,美国FDA将对Iovance Biotherapeutics公司的TIL疗法lifileucel的生物制品许可申请(BLA)做出审评决定。TIL疗法有望在35年的长跑之后,迎来首次获得FDA批准的里程碑。

TIL的优势和挑战
TIL和CAR-T细胞疗法都利用从患者体内获得的免疫细胞来治疗癌症,然而它们之间有着明显的区别。CAR-T疗法将从患者血液中获得的T细胞进行基因工程改造,在细胞表面表达识别癌细胞表面抗原的嵌合抗原受体(CAR)。当这些细胞被输注回患者体内后,它们会攻击表达这些抗原的细胞。
TIL来自从患者体内切除的实体瘤。它们已经迁移到肿瘤中并且识别癌细胞表面表达的新抗原。TIL的靶向特异性是这一疗法类型的优势,也带来它需要克服的挑战。因为TIL能够靶向肿瘤特异性新抗原,因此它们不会攻击健康细胞。而且TIL可以靶向多种新抗原,从而减少肿瘤细胞产生免疫逃逸的风险。然而,TIL的独特性以及只能从病患体内取出的肿瘤组织中取材让大规模生产这些细胞变得非常困难。
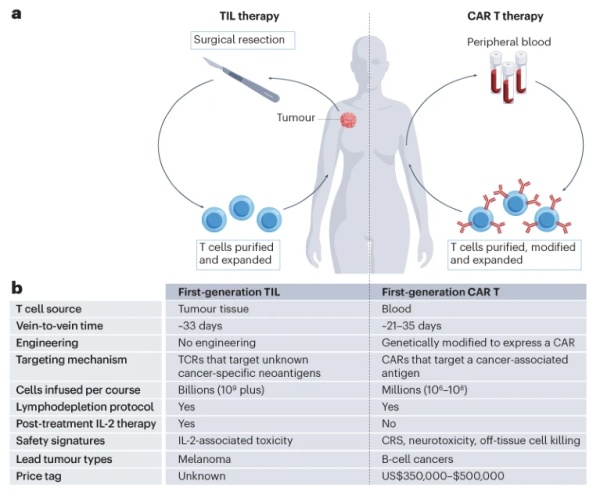
▲TIL疗法和CAR-T疗法的比较(图片来源:参考资料[1])
最初的TIL疗法需要长达8周才能完成制造,很多晚期患者在这段时间里可能疾病已经进展到无法接受治疗的程度。Iovance公司从多方面改良了TIL的生产工艺。该公司的中心化生产模式只需要22天就可以完成TIL疗法的生产过程。
治愈实体瘤的潜力
该公司的lifileucel在治疗晚期黑色素瘤患者的2期临床试验中达到31.4%的客观缓解率。这些患者已经接受过免疫检查点抑制剂的治疗,对于他们来说,可以选择的治疗手段非常有限。在这些患者中,约6%的患者达到完全缓解,获得完全缓解的患者中,有的患者已经在接受一次治疗后长达5年无癌。而且随着时间的推移,患者的缓解继续加深,7名最初被判定为部分缓解的患者后来转变为确认完全缓解。
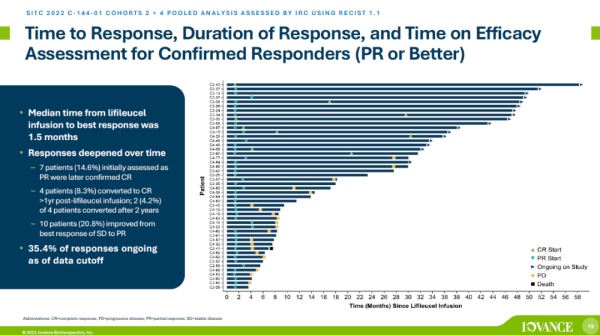
▲Lifileucel可以给部分患者通过一次治疗,带来持久缓解(图片来源:Iovance公司官网)
在2022年底公布的TIL疗法的首个大型随机3期临床试验结果显示,与抗CTLA-4抗体相比,接受TIL疗法的转移性黑色素瘤患者的无进展生存期提高了一倍。20%接受TIL治疗的患者达到完全缓解,其中有的患者已经10年无癌。“他们得到了治愈,这真是令人惊叹。”这项临床试验的研究者之一,哥本哈根大学医院的肿瘤学家Inge Marie Svane博士说。
在治疗黑色素瘤以外的其它癌症方面,TIL疗法也显示出潜力。在Nature Medicine上发表的一项概念验证1期临床试验中,TIL疗法让两名对PD-1抑制剂耐药的晚期非小细胞肺癌患者的肿瘤完全消失,并且缓解持续至少1年半。
新一代TIL疗法的发展方向
目前,多家新锐公司在致力于进一步改进TIL疗法,它们开发的多款疗法已经进入临床开发阶段。
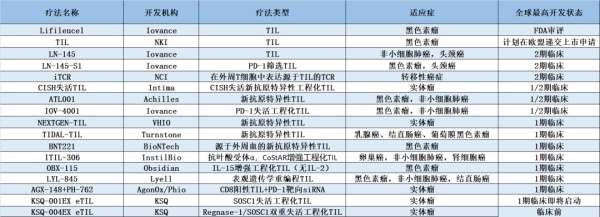
▲部分在研TIL疗法(数据来源:参考资料[1],药明康德内容团队制图)
改进TIL疗法的策略之一是筛选和扩增TIL中最具抗癌活性的细胞亚型。TIL包括多种T细胞克隆,它们有着不同的免疫特征,并且靶向不同的癌症抗原。TIL领域先驱Rosenberg博士表示,第一代TIL疗法中只有三分之一的细胞在与肿瘤细胞培养在一起的时候能够识别肿瘤细胞。“大部分输注到患者体内的细胞并没有活性,”他说,“如果能够选择具有正确特征的细胞,那将改良治疗效果。”
Achilles Therapeutics和Turnstone Biologics等新锐正在沿着这一思路迈进。它们使用各自的筛选方法筛选识别肿瘤新抗原的TIL细胞,并且对它们进行扩增。两家公司的新抗原靶向TIL疗法已经进入1期临床试验阶段。
另一种策略是通过基因工程改造TIL细胞,增强它们的抗癌活性。比如,利用基因编辑技术沉默PD-1受体的表达,可能让TIL细胞不容易受到肿瘤微环境中PD-L1的抑制,更有利于释放它们的活性。其它基因编辑的靶点包括免疫检查点蛋白CISH,抑制细胞因子信号的SOCS1等等。而KSQ Therapeutics公司的在研疗法KSQ-004EX eTIL更进一步,在让SOCS1失活的同时,还敲除了Regnase-1的表达,让T淋巴细胞更具有中央记忆干细胞的特征。
KSQ公司首席科学官Micah Benson博士表示,这些改造最终可能让更多的患者能够使用TIL疗法。TIL疗法的难点之一是患者需要患有转移性癌症,但同时又需要足够健康,能够耐受清除淋巴细胞的化疗和高剂量的IL-2。“患者体验是现今困扰TIL疗法的挑战之一。”Benson博士说。基因工程改造可能改善TIL的扩增和定植,从而扩展这一治疗模式的可及性。
迎接里程碑时刻
美国FDA预计在2024年2月24日之前对lifileucel的BLA做出审评结果。如果获得批准,将是使用细胞疗法治疗实体瘤方面的重要里程碑。TIL开发机构也尤为关注FDA对TIL疗法疗效检测手段的审评意见。与CAR-T疗法不同,TIL细胞疗法没有表达CAR的转基因,因此无法使用CAR表达水平在治疗前衡量疗法的效果。这也是lifileucel审评过程中需要克服的挑战。不过Iovance首席医学官Graf Finckenstein博士表示,通过检测多种细胞特征可以预测疗法的效果。这也是未来提高TIL疗法疗效可重复性的重要一环。TIL细胞疗法在35年之后能否冲过FDA批准的终点线?让我们拭目以待。
来源:药明康德
版权及免责声明:本网站所有文章除标明原创外,均来自网络。登载本文的目的为传播行业信息,内容仅供参考,如有侵权请联系答魔删除。文章版权归原作者及原出处所有。本网拥有对此声明的最终解释权。


{replyUser1} 回复 {replyUser2}:{content}