Nature:利用CRISPR/Cas9让小鼠恢复听力
Tmc1基因是内耳中检测声波的毛细胞发挥正常功能所必需的。携带着Tmc1基因的某种显性突变的人和小鼠经历着渐进性听力丧失。在一项新的研究中,研究人员利用CRISPR-Cas9基因组编辑策略让这个基因的突变版本失活,从而降低贝多芬小鼠模型中的这种听力丧失。相关研究结果于2017年12月20日在线发表在Nature期刊上,论文标题为“Treatment of autosomal dominant hearing loss by in vivo delivery of genome editing agents”。
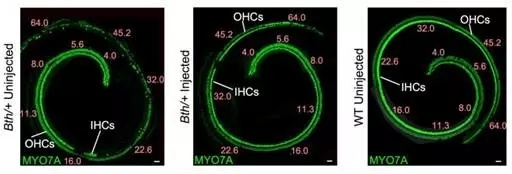 图片来自图片来自X. GAO ET AL., NATURE, 2017
图片来自图片来自X. GAO ET AL., NATURE, 2017
美国俄勒冈健康与科学大学感觉生物学家Peter Barr-Gillespie(未参与这项研究)说,“这是一项非常重要的研究。这表明CRISPR介导的基因编辑能够导致体内的听力丧失真正地改善。”
这种贝多芬小鼠模型在人Tmc1基因的小鼠版本中具有相同的点突变。大约3周后,这些小鼠开始失去一些听力,到8周时它们因它们的毛细胞死亡而变得极度耳聋。
在这项新的研究中,美国哈佛大学化学生物学家David Liu和同事们设计出一种向导RNA(gRNA)来特异性地靶向这个基因的常染色体显性的致病性拷贝。他们不是利用一种基于病毒的系统来运送Cas9和gRNA序列,而是将以一种被称作Cas9-gRNA复合体的核糖核蛋白(ribonucleotide protein, RNP)封装在脂质中并进行运送。这种策略改善了这种突变等位基因的编辑选择性,因此相比于小鼠成纤维细胞培养物中的野生型等位基因,它靶向这种突变等位基因的频率增加了20倍。
接下来,这些研究人员将脂质包装的RNP复合体注射到新生的贝多芬小鼠模型(具有一个突变等位基因和一个野生型等位基因)的一只内耳中,并留下一只未接受注射的内耳作为内部对照。这些接受注射的耳朵具有完整的健康的毛细胞,但是未接受注射的耳朵到八周时具有快速的毛细胞死亡。Liu说,“这是激动人心的,这是因为这提示着相比于未接受注射的耳朵,我们能够让接受注射的耳朵保持毛细胞健康和丰度。”
这些研究人员通过监控听觉脑干反应(auditory brainstem response, ABR)来测试四周大的贝多芬小鼠模型的听力。ABR用于衡量神经元对声音的反应。未接受注射的耳朵记录了75~80分贝左右的ABR,与垃圾处理的噪音音量相当。接受注射的耳朵能够听到安静的大约60分贝的声音,这相当于安静的谈话。尽管这是一种进步,但是野生小鼠能够听到低至30~40分贝的声音,这提示着CRISPR基因组编辑部分上避免了听力丧失。到8周时,接受注射的耳朵的ABR阈值仍然低于未接受注射的耳朵,但是要高于4周时的ABR阈值,这提示着这些小鼠的听力继续恶化。对响亮声音作出的行为反应在这些接受治疗的小鼠和野生小鼠之间遵循着类似的模式。
Barr-Gillespie说,“这远不及野生小鼠的ABR阈值,但是10~15分贝的差距可能会对人类产生巨大的影响。这种差距在人群中是非常常见的,可能导致生活质量得到实质性的改善。”
比利时列日大学神经科学家Brigitte Malgrange(未参与这项研究)说,“对治疗遗传性耳聋来说,这是令人印象深刻的,也是非常重要的结果。这是小鼠体内开展的,因此下一步将是在人体中进行测试。”
美国约翰霍普金斯大学医学院神经科学家Ulrich Müller(未参与这项研究)说,“问题在于这项技术的适用范围有多大。”他解释道,许多遗传性耳聋在人胎儿发育期间就会出现,这就是使得这种基因组编辑的运送策略更充满挑战性。但是,尽管存在一些通用性的问题,但是相比于依赖持续性病毒感染的运送策略,这些研究人员开发出的RNP复合体运送策略会降低脱靶效应产生的几率。这是它的一种优势。
Liu说,“我认为基因组编辑试剂的瞬时运送是特别有前景的,只要这样的运送策略是可行的话。对可通过局部注射运送这些试剂的眼睛和耳朵之类的组织而言,这种局部的RNP复合体运送具有一些真正的优势。”
参考资料:Xue Gao, Yong Tao, Veronica Lamas et al. Treatment of autosomal dominant hearing loss by in vivo delivery of genome editing agents. Nature, Published online: 20 December 2017, doi:10.1038/nature25164
来源:生物谷


{replyUser1} 回复 {replyUser2}:{content}